Металлический галлий
Cтраница 3
При действии избытка металлического галлия на дивинилртуть образуется тривинилгаллий. Реакцию ведут при комнатной температуре в течение 24 час. Полученный продукт выделяют кристаллизацией при низкой температуре. В чистом виде он плавится при - 7 до-9 С. Повышение температуры реакции или увеличение ее длительности приводит к снижению выхода и полимеризации продукта. [31]
Результаты анализа образца металлического галлия на элементы-примеси при 200-кратном обогащении ( табл. 3) воспроизводятся и подтверждаются полярографическим и колориметрическим методами. [32]
Растворяют 3 г металлического галлия в 30 мл соляной кислоты; избыток кислоты удаляют выпариванием. Раствор переносят в мерную колбу и водой доводят до 100 мл. [33]
Для этого над металлическим галлием при температуре около 400 С пропускают пары его трихлорида. Образовавшийся монохлорид собирается на охлаждаемом конденсаторе. [34]
Никелевую лодочку с металлическим галлием помещают в никелевую трубку и нагревают в потоке HF до 550 С. [35]
Для этого над металлическим галлием при температуре около 400 С пропускают пары его трихлорида. Образовавшийся монохлорид собирается на охлаждаемом конденсаторе. [36]
На воздухе на поверхности металлического галлия обычно образуется тонкая пленка оксида, так что дальнейшее окисление незначительно; заметнее процесс окисления идет при 500 С; при более высоких температурах металл сгорает до оксида. Галлий легко растворяется в азотной и серной кислотах, а реагируя с щелочами, образует амфотерный гидроксид. По отношению к воде галлий весьма устойчив, не разлагая ее даже при 100 СС. Галлий взаимодействует с галогенами ( кроме иода), даже на холоду образуя галогениды; с иодом галлий взаимодействует только при нагревании. [37]
Восстановление РС13 или АзС13 металлическим галлием осуществляют в кварцевой ампуле при 76 и 130 С соответственно. [38]
Получается восстановлением треххлористого гадлия металлическим галлием. [39]
Получается восстановлением треххлористого галлия металлическим галлием. [40]
Для определения индия в металлическом галлии отделяют индий соосаждением с сульфидом кобальта, затем индий переводят в дитизонат, экстрагируя его в присутствии салициловой кислоты. К экстракту добавляют соляную кислоту для разрушения дитизоната индия и после выпаривания раствора и удаления остатков органических веществ полярографируют индий на фоне 0 2 - м, соляной кислоты. [41]
По литературным данным [483], металлический галлий получается при электролизе раствора галлата натрия, содержащего 50 г / л галлия, при температуре 30 Сие применением жидкого галлия в качестве катода. Этим методом получается металлический галлий чистотой 99 9 %, дальнейшая очистка которого осуществляется методом фракционной кристаллизации азотнокислого раствора галлия. [42]
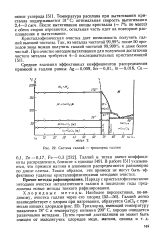 |
Система галлий - трихлорид галлия. [43] |
Наряду с кристаллофизическими методами очистки металлического галлия в последние годы предложены новые методы тонкого рафинирования. [44]
Другие методы основаны на взаимодействии металлического галлия с соответствующими ди-алкильными соединениями ртути, а также на взаимодействии трех-хлористого галлия с соединениями Гриньяра или же диалкилцин-ком. Для получения таллийтриалкилов необходимо использовать алкильные соединения лития, так как с менее реакционноспособ-ными соединениями Гриньяра будет образовываться только очень устойчивый диалкилталлийгалогенид; органические соединения ртути при взаимодействии с таллием алкильных соединений не образуют. [45]
Страницы: 1 2 3 4