Галоген
Cтраница 1
Галоген в а-положешш гидролизуется очень легко, в р-положении значительно труднее, галоген в - поло-жении очень прочен. Так, С1СН2 - О - СН2С1 моментально разлагается водой; ( С1СН2СН2) 20 ( хлорекс) гидролитически прочен, применяется в качестве растворителя, при кипячении с едкой щелочью превращается в дивиниловый эфир ( СН2СН2) 20, чрезвычайно стоек к гидролизу. Изомерный хлорексу ClCHjCHjOCHClCHg, содержащий один атом хлора в а-положении, в воде легко разлагается на этилем-хлоргидрин и ацеталъдегид. [1]
Галогены могут быть замещены алкильными или арильными группами действием реактивов Гриньяра и алкоксо-группами действием спиртов; при их гидролизе получается фосфорная кислота. [2]
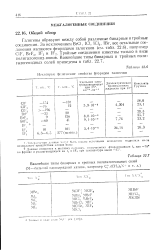 |
Некоторые физические свойства фторидов галогенов. [3] |
Галогены образуют между собой различные бинарные и тройные соединения. Тройные соединения известны только в виде полигалогенид-ионов. [4]
Галоген, стоящий в боковой цепи ароматического соединения, отличается подвижностью; галоген, находящийся в кольце, мало-реакционноспособен. [5]
Галоген - 1-ацилцикло-алканы ( XXIX) имеют склонность перегруппировываться гладко, тогда как изомерные им галогенметилциклоалкилкетоны ( XXXI) образуют продукты перегруппировки с меньшими выходами. Яркой иллюстрацией является ряд бромкетонов, производных самого ацетилциклогексана. [6]
Галоген вступает в пара-положение по отношению к группе, уже присутствующей в бензольном производном, если последняя ориентирует именно в это положение. Данные анализа, проводимого при помощи инфракрасных спектров, показали, что обычно образуется также небольшое количество орго-изомера. [7]
Галоген соединяется с водородом воды, образуя гало-геноводород; кислород воды присоединяется к сернистой кислоте. [8]
Галогены присоединяются к непредельным нитрос оединениям по гетеролитическому механизму. Так как нитрогруппа является сильным электроноакцептором, то электрофильное присоединение проходит значительно медленнее, чем в стироле. [9]
Галогены могут присоединяться по радикальному ( инициатором является свет) и по ионному механизму. При ионном галогениро-вании взаимодействие я-электронов этилена с электрофильной молекулой брома приводит к образованию я-комплекса, который превращается далее в результате образования связи между положительно заряженными атомами брома и атомом углерода в карбокатион, стабилизирующийся взаимодействием с анионом брома. [10]
Галогены могут присоединяться по радикальному ( инициатором является свет) и по ионному механизму. При ионном галогенирова-нии взаимодействие я - электронов этилена с электрофильной молекулой брома, вызывающего ее поляризацию, приводит к образованию я-комплекса, который превращается далее в результате образования связи между положительно заряженными атомами брома и атомом углерода в карбокатион. [11]
Галогены ( F, C1, Вг, I) образуют при сгорании органических веществ галогеноводороды, которые также определяются обычными способами. [12]
Галогены могут присоединяться к олефинам по радикальному или ионному механизму. [13]
Галогены также способны присоединяться к сопряженным системам в 1 2 - и 1 4-положения, причем количество 1 4-продукта зависит от строения диенового углеводорода, природы галогена и условий реакции. [14]
Галоген в галогенангидридах обладает большой реакционной способностью. При взаимодействии гаяогенангидридов с соединениями, содержащими атом металла или активный атом водорода, происходит замена его кислотным остатком. [15]
Страницы: 1 2 3 4