Галоген
Cтраница 2
Галогены и галогеноводороды легко расщепляют связь С-Sn, Соединения олова, особенно содержащие галоген, ядовиты. [16]
Галогены могут реагировать с ароматическим углеводородом тремя путями: а) присоединяться к двойным связям бензольного кольца, б) замещать водородный атом бензольного кольца с образованием галогенарила, в) замещать водородный атом в алкильной группе боковой цепи с образованием арилалкилгалогенида. [17]
Галогены относятся к заместителям первого рода, и потому при галогенировании бензола второй атом галогена вступает преимущественно в пара-положение к первому. [18]
Галогены как ориентанты в нафталиновом кольце занимают промежуточное положение между заместителями первого и второго рода. При наличии галогена в положении 1 образуются 4 - и 5-за-мещенные. [19]
Галогены при низкой температуре присоединяются к фурано-вому ядру в 2, 5-положение. [20]
Галогены химически активны, поэтому материал электродов счетчика должен эффективно противостоять газовой коррозии. Несмотря на использование галогено-уетойчивых материалов, все же имеет место1 некоторое изменение характеристик галогенных счетчиков со временем. Следует указать на более сложную технологию их производства, связанную с созданием галогеноустой-чивой пленки на деталях счетчика. [21]
Галогены в природе и кх получение. Все галогены, кроме иода, в природе в свободном виде не встречаются. Соли, в состав которых входят галогены, находятся в природе в виде залежей или в растворенном виде в воде морей, озер, буровых вод нефтеносных источников. [22]
Галогены в природе и их получение. Все галогены, кроме иода, в природе в свободном виде не встречаются. Соли, в состав которых входят галогены, находятся в природе в виде залежей или в растворенном виде в воде морей, озер, буровых вод нефтеносных источников. [23]
Галогены не присоединяются к предельным углеводородам. Однако галогены вступают с ними в реакции замещения, особенно легко на солнечном свету. При этом галогеном может последовательно заместиться не один, а несколько атомов водорода. [24]
Галоген в галогенокислотах в отличие от галогена в галогенан-гидридах связан довольно прочно. [25]
Галогены, например фтор, бром, а также хлористый и фтористый водород при комнатной температуре в отсутствие влаги не вызывают коррозии. [26]
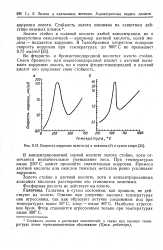 |
Скорость коррозии золота ( а и платины ( б в сухом хлоре. [27] |
Галогены в сухом состоянии, как правило, не действуют на золото. Однако при умеренно высоких температурах они агрессивны, так как образуют летучие соединения: иод при температурах выше 50 С, хлор - выше 80 С. Фтор становится агрессивным только при температурах выше 300 С. [28]
Галогены и их соединения. [29]
Галогены очень сильно различаются по своей реакционной способности ( разд. Поэтому, чтобы получить определенные фторсодержащие соединения, необходимо идти обходным путем ( разд. [30]
Страницы: 1 2 3 4