Свободный галоген
Cтраница 2
Реакция галогенирования алкенов со свободными галогенами протекает на свету и легче всего идет с хлором, несколько труднее с бромом и еще труднее с иодом. [16]
Галогенирование BmHio и Bi2Hi2 свободными галогенами, а также хлористым иодом и N-иодсукцинимидом протекает по элек-трофильному механизму. Бромирование Bi2Hi2 хлористым бромом ( смесью хлора и брома), а также фторирование газообразным фтором, идет, предположительно, по радикальному механизму. [17]
Общее - окисление галогенид-ионов до свободного галогена более сильными химическими окислителями. [18]
Газообразные галогеноводороды разлагаются с выделением свободного галогена, а в случае избытка фтора образуется фторид галогена. Энергично разлагаются и растворы галогеноводород-ных кислот. Углеводороды, аммиак, сероводород и их аналоги самовоспламеняются во фторе, образуя фтористый водород и фторид элемента. [19]
В отличие от реакции со свободными галогенами присоединение по месту разрыва двойной связи легче всего осуществляется с иодидами и труднее всего с хлоридами. [20]
Ароматические Галогенопроизводные получают обработкой ароматических углеводородов свободными галогенами на холоду в присутствии катализаторов ( FeCl3, FeBr3, A1C13) при этом атом водорода в ядре замещается на галоген. [21]
Анионы иода как восстановитель реагируют со свободными галогенами ( С12 и Вг2), с Н2О2, KMnO4, K2Cr2Oi и с другими окислителями, которые окисляют их до свободного иода. [22]
Часть образовавшегося галогеноводорода окисляется серной кислотой до свободного галогена. [23]
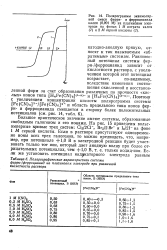
Большое практическое значение имеют системы, образованные свободным галогеном и его ионами. [24]
Большое практическое значение имеют системы, образованные свободным галогеном и его ионами. На рис. 15 приведены вольт-амперные кривые трех систем: С12 / 2С1 -, Вг2 / 2Вг - и 1г / 21 - на фоне 1 М серной кислоты. [26]
 |
Свойства простых веществ, образованных атомами галогенов. [27] |
В подгруппе с увеличением атомной массы окислительная способность свободного галогена падает. [28]
Реакции происходят также в облучаемой среде в присутствии свободного галогена, который может захватывать радикалы. [29]
В расплавленных бромидах и йодидах хлор при растворении вытесняет свободный галоген ( Вг2 или J2), который выступает в качестве непосредственного окислителя. [30]
Страницы: 1 2 3 4