Отдельный ион
Cтраница 3
Поскольку активности отдельных ионов неизвестны, то и точный расчет Афдифф по формуле ( VI. Однако если в разбавленных растворах активности отдельных ионов в первом приближении заменить их концентрациями, то, задавшись определенным распределением концентраций в области между двумя растворами, величину Дсрдифф можно рассчитать с погрешностью, которая будет тем меньше, чем более разбавленные растворы находятся в контакте друг с другом. [31]
Связь активностей отдельных ионов с активностью растворяемой соли устанавливается исходя из условия электронейтральности. [32]
Поскольку активности отдельных ионов неизвестны, то и точный расчет Афдифф по формуле (VI.27) невозможен. Однако если в разбавленных растворах активности отдельных ионов в первом приближении заменить их концентрациями, то, задавшись определенным распределением концертраций в области между двумя растворами, Афдифф можно рассчитать с погрешностью, которая будет тем меньше, чем более разбавленные растворы находятся в контакте друг с другом. [33]
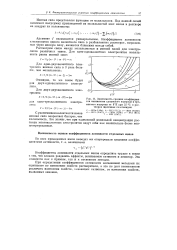 |
Зависимость средних коэффициентов активности хлористого водорода и бромистого водорода от Ym при 25 С в растворах щелочных галогенидов. [34] |
Коэффициенты активности отдельных ионов определить трудно в связи с тем, что сложно разделить эффекты, вызываемые катионом и анионом. Это относится как к прямым, так и к косвенным методам. [35]
 |
Прибор для получения сероводорода, применяемый в полумикрохимическом анализе.| Центрифуги. а - ручная. б - электрическая. [36] |
Дли обнаружения отдельных ионов обычно пользуются маленькими пробирками емкостью 2 - - 5 M. [37]
Поскольку активности отдельных ионов неизвестны, то ан осг где а - средняя активность соляной кислоты. [38]
Возможность титрования отдельных ионов и в смесях с другими ионами зависит от прочности комплекса данного иона с ЭДТА и от рН среды. [39]
А-механизм отрыва отдельных ионов; Е - гидратпровашше ионы натрия и хлора. [40]
 |
Молярные объемы некоторых форм пермутита3 при 18J. [41] |
Молярный объем отдельных ионов в ионитах в значительной степени зависит от степени сшивки обменника. [42]
Коэффициенты активностей отдельных ионов меняются в зависимости от ионной силы раствора ( /), связанной с величиной заряда ионов и концентрацией электролита. [43]
Коэффициенты диффузии отдельных ионов в растворе могут различаться, но, в силу условия электронейтральности, потоки диффузионных ионов должны быть одинаковыми, так что электролит диффундирует как целое. [44]
Высаливающее влияние отдельных ионов растет с их зарядом и уменьшается с увеличением радиуса. Рауля и падает растворимость. [45]
Страницы: 1 2 3 4