Галогенарена
Cтраница 1
Галогенарены получают прямым галогенированием аренов или замещением других групп галогеном. [1]
Галогенарены, не содержащие заместителей или содержащие электро-нодонорные заместители ( неактивированные галогенарены), реагируют лишь с очень сильными нуклеофилами-основаниями ( eNH2) или в очень жестких условиях - с водными растворами щелочей при нагревании под давлением. Особенностью этих реакций является то, что соединения, содержащие электронодонорные заместители, реагируют с образованием двух или трех изомеров. [2]
Галогенарены не вступают в большинство химических реакций, характерных для галогеналканов. Типичная для галогеналканов реакция гидролиза в ряду ароматических галогенопроизводных протекает с большим трудом. [3]
Галогенарены реагируют трудно, за исключением иодаренов. [4]
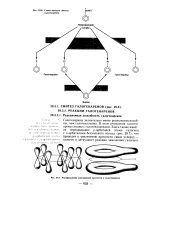 |
Схема методов синтеза галогенаренов.| Распределение электронной плотности в галогенаренах. [5] |
Галогенарены значительно менее реакционноспособ-ны, чем галогеналканы. В этом отношении галоген-арены сходны с галогеналкенами. Здесь также имеется перекрывание р-орбиталей атома галогена с л-орбиталями бензольного кольца ( рис. 29.7), что приводит к увеличению прочности связи углерод - галоген и затрудняет реакции замещения галогена. [6]
Галогенарены практически не вступают в эту реакцию. [7]
Галогенарены - довольно инертные соединения. [8]
Галогенарены с нуклеофильными реагентами взаимодействуют только при температурах выше 200 С. [9]
Галогенарены получают прямым галогенированием ароматических углеводородов и их производных. Эти реакции протекают по схеме элект-рофильного ароматического замещения ( см. разд. Некоторые галогенарены производят в промышленности в значительных количествах. [10]
Если простые галогенарены с нуклеофильнымп реагентами взаимодействуют только в жестких условиях, то для нитрованных гало-генаренов характерна высокая подвижность атома галогена. Здесь выявляется сильное электроноакцепторное влияние нитрогрупп и, кроме того, способность нитрогрупп стабилизировать промежуточные продукты реакции. Действие нитрогрупп проявляется только в о - и и-положеииях к атому галогена. [11]
Рост электронного сродства галогенарена по сравнению с бензолом соответствует снижению уровня энергии его НСМО и способствует реакциям с нуклеофильными реагентами. [12]
Если в молекуле галогенарена в о - или n - положениях находятся электроноакцеиторные группы ( N02, CN, COR), реакции нуклео-фильного замещения атома галогена проходят легче. [13]
Замещение атома галогена в галогенаренах идет только в очень жестких условиях. Примером может служить синтез фенола CeHsOH из хлорбензола. В промышленности фенол получают нагреванием хлорбензола с гидроксидом натрия до 350 С при 150 ат. [14]
С другой стороны, галогеналканы и галогенарены через стадию образования реактивов Гриньяра или литийорганических соединений могут быть превращены в твердые соединения. [15]
Страницы: 1 2