Галогениды - медь
Cтраница 2
В отличие от окислов галогениды переходных металлов проявляют значительно меньшую тенденцию к отклонениям от октаэдри-ческой координации ионов металлов. Явным исключением являются галогениды меди ( 1), в которых ион Си окружен тетраэдром из галогенов. Дифториды переходных элементов от Сг до Zn сходны с MgF2 в том, что они имеют структуру рутила. Однако в отличие от Mg2 у многих ионов переходных металлов наблюдаются искажения октаэдрической координации. Наиболее существенное искажение обнаружено для Си2 и Сг2, у которых два расстояния М - F значительно длиннее ( примерно на 20 %), чем остальные четыре расстояния, так что координацию можно описать как псевдоплоскую квадратную. Многие другие дигалогениды имеют структуры, основанные на плотноупакованных решетках галогенов с половиной занятых октаэдрических дырок. Так, в МпС12, FeCl2, СоС12, № С12, Nil3 и ZnBr2 галогенидная решетка представляет собой кубическую плотную упаковку, а в MnI2, FeBr2, FeI2, CoBr2, CoI2 и № Вг2 имеется гексагональная плотная упаковка галогенов. Многие тригалогениды сходны с дигалогенидами в том отношении, что они также основаны на плотных упаковках галогенов с катионами металлов в октаэдрических дырках. В этих случаях стехиометри-ческие соотношения требуют, чтобы была заполнена одна треть дырок. Следует отметить, что в ZnQ2 ионы цинка находятся в тетраэдрическом окружении. [16]
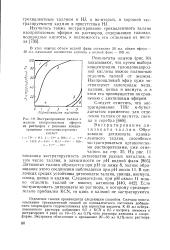 |
Экстрагирование таллия и железа изопропиловым эфиром из растворов с разными концентрациями галоидоводородных кислот. [17] |
Результаты опытов ( рис. 10) показывают, что путем выбора концентрации галоидоводород-ной кислоты можно полностью отделить таллий от железа. Изопропиловый эфир хуже экстрагирует галогениды меди, кадмия, цинка и висмута, и в этом его преимущество по сравнению с диэтиловым эфиром. [18]
Полимер, содержащий водород и галоген, разлагают при нагревании с образованием соответствующего гало-геноводорода. При смешивании пробы с окисью меди и последующем нагревании образуются галогенид меди, двуокись углерода и вода. Галогенид меди имеет характерную зеленую или сине-зеленую окраску в несветящемся спиртовом или газовом пламени. [19]
Третью группу растворителей образуют прежде всего кислоты Льюиса, способные взаимодействовать с анионами или с центрами, имеющими избыточную электронную плотность. Такими свойствами обладают двуокись серы, тригалогениды бора, тригалоге-ниды алюминия, хлорид цинка, пентагалогениды сурьмы, хлорид ртути, галогениды меди, соли серебра. [20]
Такой тип соединений известен для металлов: Си, Аи, Mn, Re, Fe, Ru, Os, Co, Rh, Ir, Pd, Pt. Эти вещества, в которых металл связан и с окисью углерода и с галоидом, могут получаться двумя путями. Галогениды меди и благородных металлов ( если надо - в присутствии восстановителя) поглощают окись углерода и образуют металлкарбонилгалогениды. [21]
Такой тип соединений известен для металлов: Си, Аи, Mn, Re, Fe, Ru, Os, Co Rh, Ir, Pd, Pt. Эти вещества, в которых металл связан и с окисью углерода и с галоидом, могут получаться двумя путями. Галогениды меди и благородных металлов ( если надо - в присутствии восстановителя) поглощают окись углерода и образуют металлкарбонилгалогениды. [22]
Полимер, содержащий водород и галоген, разлагают при нагревании с образованием соответствующего гало-геноводорода. При смешивании пробы с окисью меди и последующем нагревании образуются галогенид меди, двуокись углерода и вода. Галогенид меди имеет характерную зеленую или сине-зеленую окраску в несветящемся спиртовом или газовом пламени. [23]
Небольшую петлю на конце медной проволоки прокаливают в пламени горелки до исчезновения зеленого окрашивания пламени. После охлаждения на петлю наносят исследуемое вещество и вновь нагревают в бесцветном пламени горелки. Если вещество содержит хлор, бром или иод, образуется галогенид меди, окрашивающий пламя в зеленый цвет. [24]
Небольшую петлю на конце медной проволоки прокаливают в пламени горелки до исчезновения зеленого окрашивания пламени. Поверхность проволоки покрывается при этом слоем окиси меди. После охлаждения на петлю наносят исследуемое вещество и вновь нагревают в бесцветном пламени горелки. Если вещество содержит хлор, бром или иод, образуется галогенид меди, окрашивающий пламя в зеленый цвет. [25]
Для серебра хорошо известны все моногалогениды, плавящиеся без разложения. В то ж е время для золота моногалогениды почти не характерны. Так, монофторид золота неизвестен, а остальные неустойчивы, даже монохлорид. Энтальпия образования Aul равна 4.0 кДж / моль. Галогениды меди занимают промежуточное положение, монофторид также не существует. Из галогенидов меди в степени окисления 2 наиболее устойчив CuF2, а иодид не получен. [26]
Последние путем отжига можно перевести в кристаллическое состояние. Аморфные олово и висмут получают конденсацией паров на охлажденной подложке в присутствии примесей меди или галлия. Чистые щелочные галогениды при конденсации кристаллизуются, но стекловидный йодистый калий KI можно получить при добавлении фторида калия KF. Галогениды меди ведут себя как чистые щелочные галогениды, соответстующие же галогениды таллия можно выделить в стеклообразном виде. [27]
Моногалогениды характерны прежде всего для серебра, так как только серебро показывает устойчивую степень окисления - - J. Для серебра хорошо известны все моногалогениды, плавящиеся без разложения. В то же время для золота моногалогениды почти не характерны. Так, монофторид золота неизвестен, а остальные неустойчивы, даже монохлорид. А энтальпия образования Aul равна 4 0 кДж / моль. Галогениды меди занимают промежуточное положение, монофторид также не существует. Из галогенидов меди в степени окисления 2 наиболее устойчив CuF2, а иодид не получен. [28]
В табл. 2 дана сводка значений чисел переноса в твердых солях. Абсолютные значения чисел переноса для одной и той же соли, приводимые разными исследователями, не всегда хорошо согласуются между собой. Как ясно показано Керкгофом [12] на примере КС1, это происходит в основном из-за различия в чистоте соли. Значение таблицы, однако, состоит в выявляющейся качественной закономерности. Галогениды в основном представляют собой чисто ионные проводники, тогда как многие сульфиды и окислы ( например, a - Ag2S, PbS, NiO, Cu2O, Fe3O4) являются электронными проводниками. Тенденция окислов и сульфидов к проявлению электронной проводимости связана с наблюдаемыми для них отклонениями от стехиометрии ( см. стр. Галогениды меди представляют исключение, так как в области температур 0 - 400 их проводимость полностью переходит из электронной в катионную. Галогениды щелочных металлов, относящиеся к чисто ионным проводникам, при низких температурах обладают 100 % - ной катионной проводимостью, но при повышении температуры, когда потенциальные барьеры для движения ионов всех типов уменьшаются, начинает проявляться также анионная проводимость. Чем чище галогениды щелочных металлов, тем ниже температура, при которой становится заметной эта биполярная проводимость. [29]
Страницы: 1 2