Центральный ион - комплекс
Cтраница 2
Аналогичное превращение одного комплексного иона в другой происходит и при попадании комплексного соединения в растворитель, молекулы которого образуют с комплексообразователем более прочную связь, чем связь ли-гандов с центральным ионом растворенного комплекса. [16]
Можно не противопоставлять друг другу понятия нейтральной молекулы и кислотного остатка, но лишь учитывать, что так называемые нейтральные молекулы, вообще говоря, склонны к диссоциации с отщеплением положительных ионов за счет их отталкивания центральным ионом комплекса. [17]
Таким образом, величина отрицательного логарифма константы диссоциации комплекса может служить мерой энергии химической связи между определяемым ионом X и ионом реактива R. Обычно определяемый ион является центральным ионом комплекса, а ион ( молекула) реактива - координированным ионом или дипольной молекулой. [18]
На первый взгляд могло бы показаться, что это объяснение должно было бы быть принято во внимание в первую очередь. Однако представление о непосредственном обмене электронами между центральным ионом комплекса и электродом наталкивается на серьезные затруднения из-за симметричного окружения центрального иона отрицательно заряженными радикалами. [19]
Совершенно аналогичная ситуация имеет место во всех остальных вариантах рассматривавшихся структур - тригональных, гексагональных и ромбоэдрических. Во всех этих случаях тройная ось структуры проходит через центральный ион окта-эдрического комплекса. Ввиду отсутствия признаков искажения симметрии этих кристаллов ( как и появления сверхструктуры) приходится допускать, что тройная ось в комплексных анионах, несмотря на ее отсутствие в каждое отдельно взятое мгновение, существует в качестве статистического среднего. [20]
Ряд сделанных им обобщений эмпирического характера представляет значительный интерес. Например, им была установлена зависимость степени прочности присоединения аммиака к центральному иону комплекса от наличия в нем различных анионов. [21]
Очевидно, что комплексообразование может существенным образом повлиять на обменные реакции с участием центрального иона комплекса и лигандов. [22]
Он высказал мысль, что отщепление иона водорода от координатпвно связанной воды является следствием электростатического отталкивания иона водорода одноименно заряженным центральным ионом комплекса. [23]
Он высказал мысль, что отщепление иона водорода от координативно связанной воды является следствием электростатического отталкивания иона водорода одноименно заряженным центральным ионом комплекса. [24]
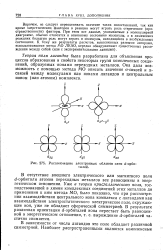 |
Расположение электронных облаков пяти rf - орби. [25] |
В отсутствие внешнего электрического или магнитного поля d - орбитали атомов переходных металлов все равноценны в энергетическом отношении. Уже в теории кристаллического поля, господствовавшей в химии комплексных соединений этих металлов до применения к ним метода МО, было показано, что при рассмотрении взаимодействия центрального иона комплекса с лигандами как взаимодействия электростатического электрическое поле, окружающее ион, уже не обладает сферической симметрией. [26]
Заряд подобного комплексного иона равен заряду центрального иона. От этого правила отступление будет только в тех случаях, когда роль молекул А играют протонсодержащие молекулы RH, способные в заметной степени диссоциировать на ионы водорода, уходящие в раствор, и ионы R, остающиеся в связи с центральным ионом комплекса. [27]
Как показали работы Есина [6, 7], Бокриса [8-10], Малкина и др., силикатные расплавы обладают анионным каркасом, состоящим из кремнекислородных, алюмокислородных и аналогичных им тетраэдров, внутри которых преобладающей является ковалентная связь. Ионы-модификаторы связаны с каркасом по преимуществу ионными связями. Заряд центрального иона комплекса в значительной степени зависит от основности расплава и уменьшается с увеличением отношения [ О ]: [ А ], где [ А ] - концентрация центрального иона, [ О ] - концентрация кислорода. [28]
Однако в основном этот реагент используется для отделения актиноидов. Экстракция координационно-ненасыщенных хе-латов ТТА служит хорошим примером синергетического влияния моно-дентатных лигандов ( стр. Во всех этих случаях центральный ион комплекса присоединяет дополнительно два мо-нодентатных лиганда. [29]
Перекись водорода образует комплексные соединения с рядом элементов; для колориметрического анализа важны комплексы с титаном, ванадием, церием, ураном и некоторыми другими металлами. Эти факторы влияют главным образом на состояние центрального иона комплекса. [30]
Страницы: 1 2 3