Галогениды - элемент
Cтраница 1
Галогениды элементов в степенях окисления 2, 3 образованы за счет полярных связей. [1]
Галогениды элементов второй группы так же, как и хлорид кобальта и иод, оказывают небольшое влияние на выход окси-кислот, но не на удельное вращение продукта. [2]
 |
Некоторые химические свойства соединений S-F. [3] |
Галогениды элементов VI группы и их основные свойства приведены в табл. 21.4. Ниже будут обсуждены только некоторые из них. [4]
Галогениды элементов V группы могут быть рассмотрены с точки зрения оценки их донорно-акцепторных свойств. В реакциях с А1С13 и ВС13 только трихлорид и трибромид фосфора проявляют заметные, хотя и слабые донорные свойства. В связи с наличием у трихлорида фосфора таких слабых акцепторных и донорных свойств, а также вследствие небольшой диэлектрической проницаемости растворяющая способность этого растворителя очень ограничена. Даже такие хорошо растворимые в большинстве галогенидов соединения, как трихлорид железа и тетраметиламмонийиодид, в этом растворителе лишь незначительно растворяются. [5]
Галогениды элементов IVA группы масс-спектрометрически изучены достаточно полно. В этих работах определены энергии последовательной диссоциации связей. [6]
Какими общими свойствами обладают галогениды элементов подгруппы титана и подгруппы германия. [7]
Помимо А1С13, применяют и другие катализаторы - галогениды элементов, являющиеся кислотами Льюиса, напр. SbFB, TiCl4, HgCl2, протонные кислоты - HF, H2S04, H3P04, полифосфорную к-ту, C1S03H, FSO3H, кислотные окислы и сульфиды, а также катионообменные смолы. Иногда протонные кислоты применяют как промоторы кислот Льюиса; роль промотора могут играть и следы воды. [8]
Третья подгруппа апротонных кислотных растворителей включает жидкие либо легкоплавкие галогениды элементов III - V групп периодической системы Д. И. Менделеева - бора, алюминия, галлия, германия, олова, сурьмы и некоторых других. Об этих апротонных соединениях уже говорилось достаточно много, чтобы безоговорочно признать за ними право входить в класс кислот и, следовательно, кислотных растворителей. [9]
Диметилхлорфосфинприсоединяет галоидпроизводные углеводородов, а также галоидпроиз-водные функциональных соединений и галогениды элементов IV, V и VI групп. [10]
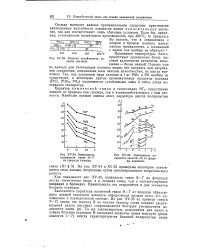 |
ЗЗ. Области устойчивости га-лидов платины.| Зависимость полярности связи Э - С1 от природы элемента. [11] |
Зависимость характера валентной связи Э - Г от природы образующего данный галогенид элемента определяется прежде всего его положением в периодической системе. Та же закономерность сохраняется для начал и концов больших периодов. [12]
Зависимость характера валентной связи Э - Г от природы образующего данный галогенид элемента определяется прежде всего его положением в периодической системе. [13]
В принципе можно осуществить реакции с такими реагентами, как галогены, ацнлхлориды, галогениды элементов ЭХП. [14]
Имея ориентировочные сведения о механизме насыщения данного металла тем или иным элементом, можно в составе насыщающей смеси использовать именно тот галогенид элемента, который участвует в основной реакции насыщения. [15]
Страницы: 1 2