Другие галогениды
Cтраница 3
Однако BF3 можно получить проще, чем другие галогениды бора; последнее время даже рекомендуется [57] получать галогениды бора с помощью фтористого бора. [31]
В некоторых случаях в качестве матрицы используют другие галогениды щелочных металлов и еще ряд веществ. [32]
Практическое применение имеют CF и CCU, другие галогениды углерода СГд используются редко. [33]
Галогениды алюминия А ] С13, А1Вгз и другие галогениды служат катализаторами в органическом синтезе. Во многих органических синтезах используют элементные бром и йод, бромид и иодид фосфора, йодистый водород. AgBr применяется для фотографии. Распыление в облаках аэрозолей Agl и РЬЬ часто используют для искусственного вызывания дождя и борьбы с градом. [34]
Фториды тиснила и сульфурила более многочисленны, чем другие галогениды этих групп. [35]
Фторид бора относится к воде иначе, чем другие галогениды бора. [36]
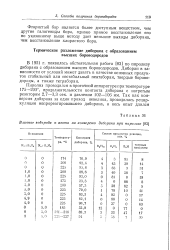 |
Влияние водорода и азота на конверсию диборана при пиролизе. [37] |
Фтористый бор является более доступным веществом, чем другие галогениды бора, однако прямое восстановление его по указанному выше методу дает меньшие выходы диборана, чем восстановление хлористого бора. [38]
 |
Строение изотактического полипропилена. [39] |
В качестве катализаторов применяют BF3, A1C13 и другие галогениды многовалентных металлов. [40]
Практически почти не реагирует с металлом CaFa и некоторые другие галогениды. [41]
Так как AgCl представляет собой осадок белого цвета, а другие галогениды серебра-осадки светложелтого цвета, обра зование Ag2CrO4 вызывает четкое изменение цвета содержимого колбы. [42]
Низшие фториды ниобия и тантала до сих пор не получены, хотя другие галогениды, в которых эти элементы находятся в состоянии низших валентностей вплоть до двух, известны. [43]
Фториды ZnF2, CdF2, HgF2 явл-яются более ионными соединениями, чем другие галогениды, и кристаллизуются в основном в структуре флюорита. Фториды - труднорастворимые вещества, менее растворимые, чем другие галогениды; относительная растворимость в ряду ZnF2 - CdF2 - HgF возрастает. Это связано не только с высокой энергией решетки фторидов, но и с тем, что для фторидов, в отличие от прочих гало-генидов, не характерно образование фторидных комплексов. [44]
Безводный тетрафторид тория ThF4 может быть получен при действии фтора или фтористого водорода на другие галогениды тория, на гидрид или карбид тория, а также при действии фтористого водорода на двуокись, гидроокись или оксалат тория. Безводный фторид тория с трудом растворяется в горячей серной и хлорной кислотах. [45]
Страницы: 1 2 3 4