Галогенуглеводород
Cтраница 1
Галогенуглеводороды являются летучими соединениями, они плохо растворяются в воде, но хорошо смешиваются со многими органическими веществами. Хладоны 114В2, 12В2 - тяжелые жидкости со специфическим запахом. Остальные хладоны при нормальных условиях - газы, легко сжижающиеся под небольшим давлением. Хладоны имеют высокую плотность как в жидком, так и газообразном состоянии, что обеспечивает возможность создания струи и проникновения капель в пламя, а также удержания паров около очага горения. Низкие температуры замерзания делают возможным применение их при минусовых температурах. [1]
Галогенуглеводороды имеют важное значение, поскольку они в большинстве своем относительно доступны и вследствие своей высокой реакционноспособности служат ценными исходными продуктами для синтеза соединений других классов. [2]
Галогенуглеводороды ( из растворителей этой группы наиболее популярен хлороформ) используют в нормально-фазовой хроматографии. Качество фармакопейного хлороформа обычно удовлетворяет основным требованиям. Следует, однако, помнить, что продажный хлороформ содержит около 1 % стабилизатора - этанола. Желательно также проводить контроль рН водной вытяжки этих растворителей, так как примеси хлороводорода способствуют коррозии аппаратуры. [3]
Галогенуглеводороды алкнлкруют ацетиламино-малоновый эфир. [4]
Галогенуглеводороды плохо растворяются в воде, но хороню смешиваются со многими жидкими органическими веществами. [5]
Галогенуглеводороды восстанавливаются на катоде до углеводородов. Галогены являются сильно электроотрицательными атомами, поэтому 5-связь С - Г ( Г С1, Вг) имеет заметное сродство к электрону. В результате на катоде сначала образуется анион-радикал, который, отщепляя галогенид Г -, превращается в радикал углеводорода. Последний, отрывая водород от растворителя HS, образует углеводород. [6]
Галогенуглеводорода в атмосфера / Soainaga Tak shi / / Кикан кагаку сосэцу. [7]
Чаще всего легкие галогенуглеводороды концентрируют из воздуха в коротких колонках с графитирован-ной сажей [320] или активным углем. [8]
Аммиак, галогенуглеводороды, спирты, органические кислоты, хлороводород, хлор, бром, оксиды азота ( до 0 5 мг / м3), озон ( до 0 6 мг / м3) не мешают определению. [9]
Медь с галогенуглеводородами при обычной температуре не взаимодействует. Медь является металлом малоактивным, кроме того, ее поверхность всегда покрыта плотным оксидным слоем. Возможность взаимодействия меди с галогенпроиз-водными при высоких температурах спорна, так как медьорганиче-ские соединения термически нестабильны. [10]
Реакции с галогенуглеводородами протекают труднее, чем с аналогичными галогенидами кремния. [11]
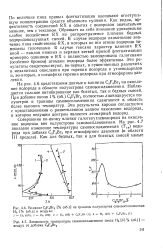 |
Влияние С2Р4Вг2 [ % ( об. ] на границы полуострова самовоспламенения Н2 [ % ( об. ] в воздухе.| Зависимость температуры самовоспламенения смеси На [ 15 % ( об. ] - воздух от добавки C2F4Br2. [12] |
Совершенно по-иному влияют галогенуглеводороды на окисление водорода вне полуострова самовоспламенения. [13]
В основе названия галогенуглеводорода лежит название самой длинной неразветвленной цепи. Атомы углерода нумеруют таким образом, чтобы меньший локант получил заместитель, который в названии пишется первым, а сами заместители перечисляются в порядке алфавита. [14]
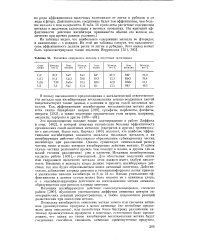 |
Расчетное содержание металла в щелочных галогенидах. [15] |
Страницы: 1 2 3 4