Галоиданизол
Cтраница 1
Галоиданизолы представляют собой соединения весьма реак-ционноспособные. Они очень легко алкилируются олефинами в присутствии ВРз и его комплексов с ортофосфорной кислотой и этиловым эфиром и образуют алкилгалоиданизолы с хорошим выходом. В ряду галоиданизолов активность падает с увеличением молекулярного веса галоида. Как и в случае талоидфенолов, наиболее активными в изученных условиях являются фторанизолы. Приблизительно такой же реакционной способностью обладают хлоранизолы, и наименее реакционноспособными являются бром-анизолы. Фтор - и хлоранизолы легче алкилируются олефинами, чем анизол и даже фенол. Со всеми изученными олефинами они образуют алкилгалоиданизолы с выходом, близким к количественному. [1]
Галоиданизолы представляют собой соединения весьма реакционно-способные. Они очень легко алкилируются олефинами в присутствии BF3 и его комплексов с ортофосфорной кислотой и этиловым эфиром и образуют алкилгалоиданизолы с хорошим выходом. В ряду галоиданизолов активность падает с увеличением молекулярного веса галоида. Как и в случае галоидфенолов, наиболее активными в изученных условиях являются фторанизолы. Приблизительно такой же реакционной способностью обладают хлоранизолы, и наименее реакционноспособными являются броманизолы. Фтор - и хлоранизолы легче алкилируются олефинами, чем анизол и даже фенол. Со всеми изученными олефинами они образуют алкилгалоиданизолы с выходом, близким к количественному. [2]
Алкилирование галоиданизолов проводилось так же, как и галоидфенолов. После прибавления рассчитанных количеств олефинов реакционная смесь перемешивалась в течение 2 - 4 час. При атмосферном давлении отгонялись растворитель и не вступившие в реакцию исходные галоиданизолы и олефины, а продукты алкилирования фракционировались в вакууме. Состав и строение их устанавливались количественным анализом на галоид и превращением в различные производные. [3]
Метоксильная группа у галоиданизолов является более сильным ориеятантом, чем атом галоида, и она ориентирует вновь вступающие алкильные радикалы в случае тг-галоиданизолов в орто-положешш, а в реакции с о-галоиданизолами в пара-положение. Такие дициклогексил-4 - галоиданизолы не способны деме-тилироваться при помощи HJ и НВг в обычных условиях вследствие блокирования метоксильной группы циклогексильными радикалами, занимающими оба орто-положедия. [4]
Метоксильная группа у галоиданизолов является более сильным ориен-тантом, чем атом галоида, и она ориентирует вновь вступающие алкильные радикалы в случае и-галоиданизолов в орто-положения, а в реакции с о-галоиданизолами в пара-положение. Поэтому при алкилировании о-галоиданизолов олефинами образуются 4-алкил - 2-галоиданизолы, а при алкилировании 4-галоиданизолов монозамещенные представляют 2-ал-кил - 4-галоиданизолы, а дизамещенные являются 2 6-диалкил - 4-галоида-низолами. Такие дициклогексил-4 - галоиданизолы не способны демети-лироваться при помощи HJ и НВг в обычных условиях вследствие блокирования метоксильной группы циклогексилышми радикалами, занимающими оба орто-положения. [5]
 |
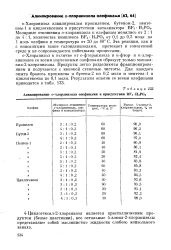
Алкилирование о-хлоранизола олефинами в присутствии BF3 Н3Р04. [6] |
Эта реакция, как и с описанными выше галоиданизолами, протекает в гомогенной среде и не сопровождается побочными процессами. [7]
В табл. 136 приводятся физико-химические константы алкилгалоиданизолов, полученных нами путем алкилирования галоиданизолов олефинами в присутствии фтористого бора и его молекулярных соединений с орто-фосфорной кислотой и этиловым эфиром. [8]
Пропилен, бутен-2, и циклогексен в реакции с фтор и хлор-анизолами проявляют приблизительно одинаковую активность; пентен-1 труднее алкилирует указанные галоиданизолы, но и он дает втор. По отношению к тг-бромфенолу бутен-2 значительно менее реакционноспособен, чем пропилен и особенно циклогексен. [9]
Пропилен, бутен-2 и циклогексен в реакции с фтор - и хлоранизолами проявляют приблизительно одинаковую активность; пентен-1 труднее алкилирует указанные галоиданизолы, но и он дает втор. По отношению к гс-броманизолу бутен-2 значительно менее реакционноспособен, чем пропилен и особенно циклогексен. [10]
Метоксильная группа у галоиданизолов является более сильным ориеятантом, чем атом галоида, и она ориентирует вновь вступающие алкильные радикалы в случае тг-галоиданизолов в орто-положешш, а в реакции с о-галоиданизолами в пара-положение. Такие дициклогексил-4 - галоиданизолы не способны деме-тилироваться при помощи HJ и НВг в обычных условиях вследствие блокирования метоксильной группы циклогексильными радикалами, занимающими оба орто-положедия. [11]
Резкого отличия в реакционной способности о - и п - фтор -, а также о - и и-хлоранизолов не наблюдается. Это объясняется возможно тем, что эти галоиданизолы с олефинами взаимодействуют почти количественно. Однако и фтор - и тг-хлоравизолы с пропиленом, бутеном-2, пентеном-1 и циклогексеном, а также о-фтор-анизол с пентеном-1 и циклогексеном при всех изученных условиях образуют по два продукта: моно - и диалкилгалоиданизолы. Причем, независимо от условий в смеси всегда преобладают моно-алкилгалоиданизолы. Диалкилгалоиданизолы образуются с выходом от 11 до 30 % и редко до 40 %: от теоретического. Хлорани-зол в различных условиях со всеми указанными олефинами дает лишь один моноалкилхлоранизол с выходом, приблизительно равным общему выходу моно - и диалкилгалоиданизолов, образующихся в реакции с о - и тг-фторанизолами и тг-хлоранизолом. [12]
 |
Алкилирование о-хлоранизола олефинами в. присутствии ВРз - НзРС4. [13] |
Эта реакция, как и с описанными выше галоиданизолами, протекает в гомогенной среде и не сопровождается побочными процессами. [14]
Резкого отличия в реакционной способности о - и тг-фтор -, а также о-и тг-хлоранизолов не наблюдается. Это объясняется, возможно, тем, что эти галоиданизолы с олефинами взаимодействуют почти количественно. Однако n - фтор - и ге-хлоранизолы с пропиленом, бутеном-2, пентеном-1 и циклогексеном, а также о-фторанизол с пентеном-1 и циклогексеном при всех изученных условиях образуют по два продукта: моно - и диалкил-галоиданизолы. Причем независимо от условий в смеси всегда преобладают моноалкилгалоиданизолы. Диалкилгалоиданизолы образуются с выходом от 11 до 30 % и редко до 40 % от теорет. Хлоранизол в различных условиях со всеми указанными олефинами дает лишь один моноалкилхлорани-зол с выходом, приблизительно равным общему выходу моно - и диал-килгалоиданизолов, образующихся в реакции с о - и тг-фторанизолами и тг-хлоранизолом. [15]
Страницы: 1 2