Галоидофторид
Cтраница 1
Галоидофториды превращают окиси во фториды и оксифториды. При действии на галоидные соли образуются фториды металлов, причем выделяется галоид. Галоидофториды окисляют такие вещества, как аммиак, гидразин, окись углерода, двуокись серы и аммонийные соли. В качестве иллюстрации в табл. 7 и 8 приведены соответствующие данные для кобальта. [1]
Самоионизация галоидофторидов доказана при помощи измерения электропроводности и методом кондуктометрического титрования растворов различных фторидов. Кроме того, известно большое число комплексных соединений со сложными анионами и катионами, возникающими в процессе ионизации галоидофторидов. [2]
Большой интерес галоидофториды представляют с точки зрения применения некоторых из них в качестве окислителей ракетных топлив и исходных соединений для их синтеза. [3]
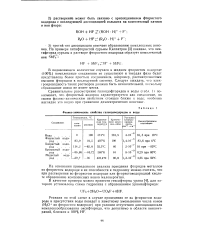 |
Физико-химические свойства галоидоводородов и воды. [4] |
Сравнительное рассмотрение галоидофторидов и воды ( табл. 1) показывает, что фтористый водород характеризуется как соединение, по своим физико-химическим свойствам стоящее ближе к воде; особенна наглядно это видно при сравнении диэлектрических констант. [5]
В ряду галоидофторидов три-фторид хлора имеет наименьшую электропроводность. Это указывает на ковалентный характер его связи и находится в соответствии со сравнительно низкой температурой кипения. [6]
Из всех галоидофторидов пентафторид иода имеет наибольшее значение для получения органических фторпроизводных. Реакция JF5 с четырехбромистым углеродом начинается лишь при нагревании до 90 С. Трихлорфторметан CC13F дальнейшему фторированию пентафторидом иода подвергается лишь с большим трудом при 125 - 225 С. [7]
Практическое применение галоидофторидов обусловлено главным образом возможностью использования их в качестве фторирующих агентов. [8]
Реакции между галоидофторидами, с одной стороны, и хлрром, бромом и иодом, с другой, протекают быстро. Однако природа получающихся продуктов и данные по равновесиям соответствующих реакций еще не установлены. [9]
По реакционной способности галоидофториды можно расположить приблизительно в следующем порядке: трифторид хлора, пентафторид брома, гептафторид иода, монофторид хлора, трифторид брома, пентафторид иода, монофторид брома. Наиболее реакционноспособным является трифторид хлора. Большинство имеющихся в литературе данных относится только к качественной характеристике зтих веществ и в некоторых случаях не является достаточно удовлетворительным. Однако приведенные ниже данные дают некоторое представление о наиболее важных свойствах этих соединений. [10]
Результаты изучения ЯМР галоидофторидов подтверждают этот порядок для относительных скоростей обмена и таким образом доказывают, что обмен в этих системах происходит именно через механизм димери-зации. [11]
Для качественной идентификации галоидофторидов применяют также инфракрасную спектроскопию и спектроскопию комбинационного рассеяния. Высокая реакционная способность этих соединений, однако, требует создания специальных приспособлений для проведения измерений. [12]
Помимо изучения химии галоидофторидов, внимание ученых привлекло исследование структуры галоидофторидов и их комплексов. [13]
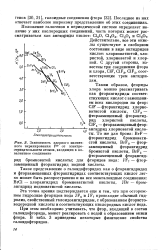 |
Зависимость ядерного магнитного экранирования F19 от электроотрицательности атомов, входящих в ко-валентное соединение. [14] |
Такое представление о галоидофторидах как о фторангидридах и фторзамещенных фторангидридах соответствующих кислот легко может быть распространено и на все межгалоидные соединения: BrCl - хлорангидрид бромноватистой кислоты, JBr - бром-ангидрид иодноватистой кислоты. [15]
Страницы: 1 2 3 4