Высокозарядный ион
Cтраница 1
 |
Степень адсорбции ионов ThB2 на осадках CaSO4 и Agl. [1] |
Высокозарядные ионы адсорбируются сильнее, чем ионы с меньшим зарядом. [2]
 |
Полярограмма смеси растворов солей кадмия, цинка и марганца.| Полярограмма ступенчатого восстановления хромата. [3] |
Высокозарядные ионы металлов способны восстанавливаться ступенчато и давать несколько полярографических волн. Это характерно, например, для анионов хромата, молибдата, вольфрамата, ванадата, катионов железа ( III), кобальта и др. На рис. 25.8 показано восстановление хромат-ионов в растворе гидроксида аммония. Высшая степень окисления образует волну при более положительном потенциале, чем средняя ( или низшая) степень окисления. Это явление иногда используют для устранения влияния посторонних ионов. Так, никель ( II восстанавливается легче кобальта ( II) и мешает определению последнего. [4]
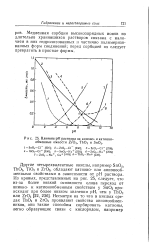 |
Влияние рН раствора на анионо - и катионо-обменные емкости ZrO2, ThO2 и SnO2. [5] |
Медленная сорбция высокозарядных ионов из длительно хранившихся растворов связана с наличием в них гидролизованных и частично полимеризо-ванных форм соединений; перед сорбцией их следует превратить в простые формы. [6]
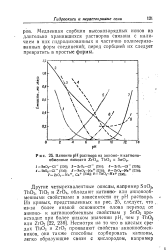 |
Влияние рН раствора на анионо - и катионо-обменные емкости ZrO2, ThO2 и SnO2. [7] |
Медленная сорбция высокозарядных ионов из длительно хранившихся растворов связана с наличием в них гндролизованных и частично нолимеризо-ванных форм соединений; перед сорбцией их следует превратить в простые формы. [8]
Однако даже для высокозарядных ионов значение п не превышает 30, а для полярных частиц составляет несколько единиц. Тем не менее в полярных растворителях все частицы сольватированы, т.е. существуют в форме комплексов. Наибольшее различие в поведении частиц в газовой фазе и в растворах проявляется для молекул с сильнополярной связью или в ионизирующих растворителях. Такими растворителями являются те, молекулы которых включают атомы с неподеленными парами электронов и обладают высокой диэлектрической проницаемостью. [9]
В этом источнике образование высокозарядных ионов происходит в результате длительного ( сотни мс) времени взаимодействия низкозарядных ионов с интенсивным электронным пучком с энергией в неск. Такие времена взаимодействия обеспечиваются удержанием ионов в потенц. [10]
Определению селена и теллура мешают высокозарядные ионы, которые подвергаются гидролизу и выделяются в виде основных солей. Если вести восстановление в очень кислой среде, то, вместе с селеном и теллуром может выделяться мышьяк. При содержании золота свыше 10 г / т его необходимо предварительно отделить. [11]
Второе правило, которому обычно подчиняются комплексные кристаллы, устанавливает, что высокозарядные ионы располагаются далеко друг от друга. Это правило является выражением требования низкой величины электростатического потенциала. Относительной нестабильности цепочек с формулой S03 может быть дано и иное толкование, чем изложенное выше. Так как S6 - высокозарядный ион и так как такие ионы в цепочке подходят очень близко друг к другу, цепь должна быть неустойчивой. [12]
Кроме получения ионов непосредственно из источника, возможен и др. метод генерации высокозарядных ионов. Ускоренные тяжелые ионы при прохождении через тонкую мишень ( газовую или твердотельную) в результате взаимодействия с атомами мишени теряют часть электронов и увеличивают свое зарядовое состояние. Величина равновесного заряда растет с энергией ионов, а дисперсия распределения d падает с ее увеличением. Этот метод получения высокозарядных тяжелых ионов, называемый обдиркой, широко используется и является основой для создания больших ускорительных комплексов разл. [14]
Высокая избирательность ионообменного процесса может быть достигнута за счет способности ионообменника лучше извлекать из разбавленных растворов высокозарядные ионы, а также при использовании хелатных смол. Однако наиболее эффективный способ повышения избирательности основан на применении комплексообразователей. [15]
Страницы: 1 2 3
