Высокозарядный ион
Cтраница 2
Купферон ( аммониевая соль N-нитрозофенилгидроксиламина) применяется в основном как групповой осадитель и экстрагент для извлечения высокозарядных ионов ряда металлов из сильнокислого раствора. Образующиеся осадки обычно недостаточно устойчивы и непригодны для непосредственной сушки и взвешивания, поэтому их приходится прокаливать до окислов. [16]
Молекулы кристаллизационной воды в таких солях во многих случаях можно считать лигандами, что особенно справедливо для переходных и высокозарядных ионов непереходных элементов. [17]
Вероятность образования иона с зарядом Z в результате одиночного электронного удара быстро уменьшается с увеличением Z, поэтому для получения достаточно эффективного выхода высокозарядных ионов используют процессы многократной ионизации. Для этого необходимо увеличить время пребывания ионов в облаке плазмы, содержащей горячие электроны. Кроме того, для образования высокозарядных ионов должно выполняться условие п / по5S 1, т.е. плотность плазмы п должна превосходить плотность нейтрального газа HO, чтобы свести до минимума захват электронов в результате столкновений. [18]
Реагенты типа а-нитрозо-р-нафтола неспецифичны и взаимодействуют подобным образом с Fe ( III), Zr ( IV), Cr ( III), W ( VI) и рядом других трех - и более высокозарядных ионов. [19]
В кислой среде с дитизоном взаимодействуют ионы многих металлов ( Те, Ag, Cu, Hg, Аи и др.), мешающие определению селена. Высокозарядные ионы, которые легко подвергаются гидролизу ( W, Nb, Та, Bi, Sn) также мешают определению селена. [20]
В этой и последующих работах даются радиусы ионов ( в А), определенные опытным путем, в скобках - вычисленные теоретически. Высокозарядные ионы ( от 4 и выше) в растворах практически не существуют. [21]
 |
Комплексные соединения с центральными атомами разного заряда. [22] |
Они определяют устойчивость возникающего комплекса, что можно проиллюстрировать простой электростатической моделью. Высокозарядные ионы малого размера образуют устойчивые комплексы. [23]
Известны многочисленные методы титрования почти всех металлов, образующих комплексы с ЭДТА. Цирконий, висмут и другие высокозарядные ионы образуют прочные комплексы и титруются в кислой среде. ЭДТА и в определенных условиях титруют остаток ЭДТА, например, солью цинка. Цинк, никель, свинец и другие двухзарядные ионы образуют менее прочные комплексы и титруются только в слабокислой среде. Еще менее прочные комплексы образуют кальций и магний, которые титруются в щелочной среде. Обычно для этого берут буферную смесь из гидроокиси аммония и хлористого аммония. [24]
Наоборот, ионы, обладающие деструктурирующим действием ( К, МОз и др.), оказывают разрыхляющее влияние на приионную зону соль-ватов. Последнее делает понятным отсутствие высокозарядных ионов в водных растворах. Так, растворение солей Со3 не приводит к образованию Со3 ( р) - происходит окислительно-восстановительный процесс, сопровождающийся выделением кислорода. [25]
Известны многочисленные методы титрования почти всех металлов, образующих комплексы с ЭДТА. Цирконий, висмут и др. высокозарядные ионы образуют прочные комплексы и титруются в кислой среде. ЭДТА и в определенных условиях титруют остаток ЭДТА, например, солью цинка. Цинк, никель, свинец и др. двухзарядные ионы образуют менее прочные комплексы и титруются только в слабокислой среде. Еще менее прочные комплексы образуют кальций и магний, которые титруются в щелочной среде. Обычно для этого берут буферную смесь из гидроокиси аммония и хлористого аммония. [26]
При ионном обмене на сильнокислотных сульфокатиони-тах и сильноосновных анионитах, а также неорганических ионообменниках, не обладающих комплексообразующими свойствами наблюдается только электростатическое притяжение ионов к ионогенным ( фиксированным) группам ионита. Поэтому можно ожидать более селективное поглощение высокозарядных ионов по сравнению с низкозарядными, если радиусы соответствующих гидратированных ионов не слишком различаются. [27]
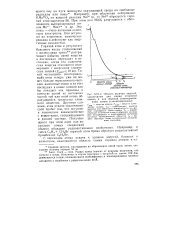 |
Область величин энергий, характерных для химии горячих атомов и для обычной ( эпитермаль. [28] |
Например, при облучении нейтронами КМп65О4 по ядерной реакции Mn55 ( n, v) Mn58 образуется горячий атом марганца-56. При этом ион MnOi разрушается с образованием высокозарядных ионов Мп 7, МпО 6 и др. Эти ионы - очень активные акцепторы электронов. Они вступают во вторичные химические реакции и действуют как энергичные окислители. [29]
 |
Зависимость максимальной кинетической энергии тяжелых ирыов от массы для различных линейных ускорителей.| Схема каскадного способа ускорения тяжелых ионов в циклотроне. [30] |
Страницы: 1 2 3