Гидро-ксильный ион
Cтраница 1
Гидро-ксильные ионы связывают водоридные ионы индикатора. Таким обра юм диссоциация индикатора усиливается. Если же прибавлять гидроксил-ионы очень маленькими порциями ( разбавленные растворы или слабые основания), то можно заметить в интервале рН от 8 до 10 переход бесцветного раствора красный. [1]
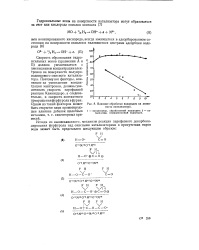 |
Влияние обработки водородом на активность катализатора. [2] |
Скорость образования гидро-ксильных ионов ( уравнения А и Б) должна увеличиваться с уменьшением концентрации электронов на поверхности полупроводникового окисного катализатора. Поэтому все факторы, влияющие на уменьшение концентрации электронов, должны увеличивать скорость парофазной реакции Канниццаро, а следовательно, и скорость контактного превращения фурфурола вфуран. [3]
 |
Абсолютные скорости v [ в см2 / ( В сек ] ионов при. [4] |
Выделяются высокие зшачелия скорестей водородных и гидро-ксильных ионов. [5]
Центральный ион комплекса может присоединять гидро-ксильные ионы с образованием основных солей или гидроокисей и при этом ослабляется или исчезает окраска раствора. [6]
Смолы-аниониты могут обменивать анионы ( гидро-ксильные ионы) на анионы солей, присутствующие в растворе. [7]
Аналогично можно объяснить большую подвижность гидро-ксильных ионов, только в этом случае переход протонов происходит не от ионов гидроксония к молекулам воды, а от молекул воды к ионам гидроксила, что приводит к кажущемуся перемещению ионов гидроксила по направлению к аноду. [8]
Известно, что произведение концентрации водородных и гидро-ксильных ионов - число постоянное. [9]
Это уравнение описывает специфический катализ гидро-ксильным ионом в противоположность уравнению ( 6), которое применимо к общему основному катализу, производимому присутствующим в растворе каким-либо веществом В. Какое из этих двух уравнений, ( 6) или ( 9), будет выполняться, зависит от относительных величин / г2 [ СН3СНО ] и & i [ BH ], и поэтому будет ли карбанион HCOCHJ реагировать более быстро с ацетальдегидом или с ВН, зависит от относительных констант скоростей и концентраций. [10]
В случае гидролиза эфира под действием водородных и гидро-ксильных ионов, согласно теории Лаури в ее современном виде, должны получаться приведенные ниже комплексы [10], которые слишком нестойки, чтобы v достигало всегда величины насыщения. [11]
Поскольку наблюдаемое значение для реакции с гидро-ксильным ионом было равно 0 919, а значение, рассчитанное с помощью уравнения ( 6), вероятно, представляет собой некоторый верхний предел силы изотопного эффекта, полученное согласие величин является не очень плохим. [12]
После прибавления к этому раствору щелочи ее гидро-ксильные ионы начинают взаимодействовать с водородными ионами кислоты, связываясь с ними в молекулы воды. Но уход ионов водорода из раствора нарушает указанное выше равновесие, вызывая диссоциацию новых молекул синильной кислоты, и таким образом постепенно вся синильная кислота диссоциирует, а освобождающиеся ионы водорода соединяются с гидроксиль-ными ионами, образуя молекулы воды. [13]
Фактически это означает, что реакция катализируется гидро-ксильными ионами. Механизмы реакций, соответствующие общей схеме ( 1 - 57), относят к типу специфического основного катализа, поскольку кажущиеся скорости таких реакций зависят только от концентрации гидроксильных ионов. [14]
В растворах, содержащих основания, соответственно влияют гидро-ксильные ионы. [15]
Страницы: 1 2 3 4