Гидро-ксильный ион
Cтраница 3
Следовательно, анионит, приведенный в равновесие с раствором углекислого калия, содержит не только карбонатные, но и гидро-ксильные ионы, а поэтому и обладает повышенной электропроводностью. [31]
Из сказанного выше следует, что катионами всегда являются ионы водорода, металлов и ионы аммония, а анионами - гидро-ксильные ионы и ионы кислотных остатков. [32]
Тем не менее, фторидный ион может и не восстанавливаться, а оставаться в дикремневой кислоте на месте одного из гидро-ксильных ионов. [33]
Аналогично на участке в при увеличении положительного потенциала ( при прямом ходе кривой) наряду с заряжением двойного слоя происходит разряд гидро-ксильных ионов и адсорбция образующихся атомов кислорода, а при уменьшении положительного потенциала - ионизация и, следовательно, десорбция кислорода. [34]
Согласно вышеуказанному, все не растворимые в воде основания должны растворяться в кислотах, ибо водородные ионы кислот выводят из сферы равновесия гидро-ксильные ионы, находящиеся в равновесии с молекулами растворенной части осадка. На этом же основании не растворимые в воде кислоты должны растворяться в щелочах. [35]
В первом случае вследствие интенсивного разряда ионов водорода на катоде в прикатодном слое электролита, граничащем с поверхностью обрабатываемых деталей, происходит обогащение гидро-ксильными ионами, которые омыляют жиры животного и растительного происхождения. [36]
 |
Схема структуры молекулы исшита. [37] |
Когда положительным подвижным ионом катионита является ион водорода - Н, то такой катионит является по существу многовалентной кислотой, так же как анионит с обменным гидро-ксильным ионом - ОН является многовалентным основанием. Подвижность способных к обмену ионов ограничивается расстояниями, при которых не теряется ьзаимосвязь их с неподвижными ионами противоположного заряда на поверхности ионита. Это ограниченное вокруг молекулы ионита пространство, в котором находятся подвижные и способные к обмену ионы, называют ионной атмосферой ионита. [38]
При взаимодействии элемента, стоящего в ряду напряжений выше водорода, с водой водородные ионы отдают свой заряд образующимся металлическим ионам, и последние, встретив гидро-ксильные ионы, образуют с ними гидроокись металла. [39]
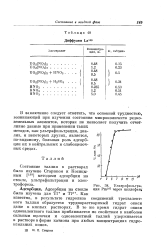 |
Диффузия Lai. [40] |
В то же время гидрат окиси одновалентного таллия приближается по свойствам к наиболее сильным щелочам и одновалентный таллий удерживается в растворе в форме катиона при любых концентрациях гидро-ксильных ионов. [41]
Из их исследования видно, что сурьмяный электрод, предложенный ими, они применяли исключительно как индикатор, не задаваясь вопросом, какова зависимость между концентрацией водородных или гидро-ксильных ионов и потенциалом электрода. [42]
С увеличением силы кислоты НА удельные скорости обоих процессов возрастают, но при данном буферном отношении скорость реакции ( Ша) в отличие от удельной скорости уменьшается, так как концентрация гидро-ксильных ионов снижается быстрее, чем возрастает удельная скорость. Поэтому возможно, что реакция ( V) протекает быстрее, чем реакция ( III), и при этом имеет удельную скорость, которая возрастает с увеличением силы кислоты НА. [43]
Реакция титрования может быть представлена следующей схемой: НА ОН - Н2О А -, где А - [ соль ], а [ НА ] - [ органическая кислота ]; прибавляемые гидро-ксильные ионы тотчас же расходуются, так что [ ОН - ] создается за счет диссоциации воды. [44]
 |
Схема приготовления и дозирования аммонийной соли ЭДТА в питательную воду. [45] |
Страницы: 1 2 3 4