Гаптоглобин
Cтраница 1
Гаптоглобин входит в состав глобулиновой фракции. Этот белок обладает способностью соединяться с гемоглобином. Образовавшийся гаптоглобин - гемоглобиновый комплекс может поглощаться системой макрофагов, при этом предупреждается потеря железа, входящего в состав гемоглобина как при физиологическом, так и при патологическом его освобождении из эритроцитов. Установлено, что имеется связь между наследованием типов гаптоглобинов и резус-антителами. [1]
Для иммобилизованного гаптоглобина на 1 моль гапгоглобина связывается в комплекс только 0 39 моль гемоглобина. [2]
Оценка размаха функциональных вариаций гаптоглобина у горожан в зависимости от фенотипа в условиях техногенного воздействия среды обнаружила разнонаправленный характер изменения концентрации белка, корреляция роста количественного содержания этого протеина с свойствами организма [4] позволяет предположить выраженный адаптационный ответ на токсическое действие городской среды. [3]
Изучение механизма взаимодействия между гаптоглобином человека, ковалентно связанным с сефарозой 4В, и гемоглобином человека, а также а - и р-цепями, обработанными я-хлормеркурибен-зоатом, проводилось двумя способами: изучалось связывание с помощью хроматографии на колонке и связывание а-цепей в равновесных условиях. Цепи - это цепи, меченные 14С с помощью п-хлормеркури - 14С ] бензойной кислоты. Связывание гемоглобина и а - и р - цепей на иммобилизованном гаптоглобине ( 38 нмоль гаптоглобина на 1 мл сефарозы 4В) показано на рис. 11.3. Добавление возрастающих количеств гемоглобина приводит к плато насыщения при 1 5 моль гемоглобина на 1 моль гаптоглобина. [4]
Максимальное число центров связывания, найденное для иммобилизованного гаптоглобина, согласуется с известным значением - четыре центра на 1 молекулу гаптоглобина в растворе. Следовательно, гаптоглобин, присоединенный к агарозе, в целом обладает теми же свойствами по связыванию гемоглобина н его а - и ( З - цепей, что и в растворе, и вследствие этого пригоден для детального исследования механизма взаимодействия между гаптоглобином и гемоглобином или его субъединицами. [5]
Из этих данных следует тот же ряд аффин-ностей для иммобилизованного гаптоглобина, что и для свободного, а именно гемоглобина-цепьр-цепь. [6]
 |
Количество р-липопротеидов в сыворотке крови крыс и удельная радиоактивность ( 72 ч после облучения в дозе 309 6 мКл / кг. [7] |
Другим компонентом а-глобулиновой фракции, наиболее подверженным постлучевым изменениям, является гаптоглобин. Анализ аминокислотного состава, пептидных карт ферментативных гидролизатов, углеводных компонентов и иммунных свойств позволил прийти к выводу о том, что первичная структура таптоглобина и его физико-химические свойства при лучевом поражении не меняются. Возрастание концентрации этого белка в сыворотке крови, по мнению А. В. Поспеловой, обусловливается усилением его синтеза клетками печени. [8]
Максимальное число центров связывания, найденное для иммобилизованного гаптоглобина, согласуется с известным значением - четыре центра на 1 молекулу гаптоглобина в растворе. Следовательно, гаптоглобин, присоединенный к агарозе, в целом обладает теми же свойствами по связыванию гемоглобина н его а - и ( З - цепей, что и в растворе, и вследствие этого пригоден для детального исследования механизма взаимодействия между гаптоглобином и гемоглобином или его субъединицами. [9]
Максимальное число центров связывания, найденное для иммобилизованного гаптоглобина, согласуется с известным значением - четыре центра на 1 молекулу гаптоглобина в растворе. Следовательно, гаптоглобин, присоединенный к агарозе, в целом обладает теми же свойствами по связыванию гемоглобина н его а - и ( З - цепей, что и в растворе, и вследствие этого пригоден для детального исследования механизма взаимодействия между гаптоглобином и гемоглобином или его субъединицами. [10]
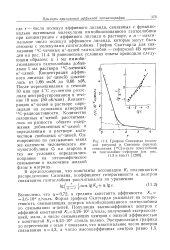 |
Графики Скатчарда ( основной рисунок и Сипсиана ( врезка связывания [ 14С1а - цепн гемоглобина на гаптоглобин-сефарозе ( и текст. [11] |
Вычислено, что а 0 72, а средняя константа аффинности Ка 3 6 - 104 л / моль. Форма графика Скатчарда указывает на гетерогенность связывающих центров иммобилизованного гаптоглобина по связыванию а-цепей. Популяция высокоаффинных центров с аффинной константой / d 5 26 - 105 л / моль, полученной экстраполяцией, мала, а число связывающих центров с низкой аффинностью с константой / ( 2 6 23 - 1 04 л / моль велико. [12]
Состарившиеся эритроциты фагоцитируются макрофагами в основном в селезенке, а также в костном мозге и печени. Гемоглобин, освобождающийся из эритроцитов в крови, связывается с гаптоглобином ( а2 - глобулин плазмы крови) и транспортируется в клетки ретикулоэндотелиальной системы ( РЭС), главным образом селезенки. [13]
Лектин из зародышей пшеницы связывает N-ацетилглюкозами-нильные остатки. Помимо очистки и фракционирования полисахаридов или гликопротеидов, сс2 - макроглобина, гаптоглобина и церу-плазмина из плазмы, секреторных гликопротеидов типа муцина, этот лектин находит применение для разделения целы - клеток ( по их поверхностным характеристикам), например T-J имфоцитов, а также клеточных органелл. Сферические гранулы диаметром 200 - 300 мкм не препятствуют свободному передвижению целых клеток с подвижной фазой. Аффинная сорбция клеток идет только на поверхности гранул. Аналогичный лектин фирмы PL-biochemicals закреплен в гранулах агарозы обычных размеров. [14]
Во времени установлен рост патологических исходов беременностей, отягощенных мутационной компонентой. Обнаружены сдвиги в распределении частот адаптивно значимых белковых маркеров и количественном содержании гаптоглобина, свидетельствующие о существенном адаптационном ответе популяции на воздействие экзогенных факторов. [15]
Страницы: 1 2