Макромолекулярный ион
Cтраница 1
Макромолекулярные ионы смещают равновесие процесса вследствие различия их влияния на прямую и обратную реакции. [1]
Эффект ускорения реакции добавками макромолекулярных ионов значительно выше, чем при добавках низкомолекулярных соединений. [2]
Из сказанного выше следует, что макромолекулярные ионы ускоряют реакцию, понижая свободную энергию активированного комплекса. В то же время добавки замедляют реакцию стабилизацией реагентов вследствие электростатического взаимодействия между макроионами, реагентами и активированными комплексами. Существующая теория Маннинга и формула Бренстеда - Бьеррума хорошо описывают это взаимодействие при малых концентрациях добавок макроионов. Однако необходимо еще объяснить сильное каталитическое действие при больших концентрациях добавки. [3]
На рис. 3.1 и 3.2 показано влияние различных макромолекулярных ионов на ход этих реакций. Из рисунков видно, что добавление катионного полимера - гидрохлорида полиэтиленимина, PEI - HC1 ( /), значительно ускоряет протекание реакции (3.1), в то время как добавка анионного полиакри-лата натрия, NaPAA ( 2), не оказывает почти никакого влияния. Отсутствие эффекта ускорения при добавке NaPAA объясняется тем, что при высокой кислотности системы добавка не диссоциирует. [4]
В дальнейшем роль такого иона может выполнить образовавшийся даже макромолекулярный ион. [5]
Электростатическое взаимодействие зависит прежде всего от зарядов реагента и макромолекулярного иона. Наблюдаемые эффекты значительно усиливаются для веществ с большим зарядом. Например, реакция переноса электрона между Fe2 и ионами Со ( МН3) 5С12, Co ( NH3) 5Br2, Co ( NH3) 5N ускоряется при введении NaPES в 103 раз, в то время как та же добавка при тех же концентрациях повышает скорость реакции между Fe2 и однозаряженными ионами транс - Co ( ea) 2Cl2 или i / uc - Co ( NH3) 4 ( N3) 2 ( en - этилендиамин) всего в 20 раз. [6]
Более низкое значение соответствует заряду ( 2) для макромолекулярного иона с молекулярным весом 10 000 при концентрации I г на 100 г растворителя или заряду ( 20) для макромолекулярного иона с молекулярным весом 100 000 при той же весовой концентрации. Такие величины заряда характерны обычно для растворов белков вблизи их изоэлектрических точек. [7]
Таким образом, кристаллы состоят [ из последовательных слоев макромолекулярных ионов противоположных зарядов. [8]
Реакции между одноименно заряженными ионами значительно ускоряются при введении в систему макромолекулярных ионов противоположного знака. [9]
Однако эти вещества при растворении в воде переходят в метаниобаты NaNb03 с макромолекулярными ионами. [10]
Очевидно, что описанное каталитическое действие связано с электростатическим взаимодействием заряженных реагентов и макромолекулярных ионов, поскольку взаимодействие всех других видов в таких системах значительно слабее. Это следует и из того факта, что добавка сополимера со структурой 5 ( RjR2 CH3) при одинаковых концентрациях оказывает в реакции (3.1) ускоряющее действие того же порядка. Эти две макромолекулярные добавки являются катионами, однако их химические структуры ( а следовательно, и распределение плотности электрических зарядов) значительно различаются, что и указывает на определяющую роль чисто электростатического взаимодействия. [11]
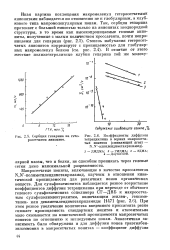 |
Сорбция гепарина на гете-росетчатом анионите.| Коэффициенты диффузии. [12] |
Иная картина поглощения макромолекул гетеросетчатыми анионитами наблюдается по отношению не к глобулярным, а клуб-кового типа макромолекулярным ионам. [13]
Более низкое значение соответствует заряду ( 2) для макромолекулярного иона с молекулярным весом 10 000 при концентрации I г на 100 г растворителя или заряду ( 20) для макромолекулярного иона с молекулярным весом 100 000 при той же весовой концентрации. Такие величины заряда характерны обычно для растворов белков вблизи их изоэлектрических точек. [14]
Синтетические сорбенты-иониты представляют полимерную матрицу с трехмерной структурой макромолекул, имеющую ионогенные группы. В растворе иониты образуют неподвижные макромолекулярные ионы и подвижные ионы противоположного знака. В зависимости от типа подвижного иона иониты делят на катиониты - поликислоты, способные обмениваться с раствором катионами, и аниониты - полиоснования, обменивающиеся с раствором анионами. [15]
Страницы: 1 2