Равновалентный ион
Cтраница 1
Равновалентные ионы также адсорбируются неодинаково в связи с отличиями в размерах и степени гидратации. По их способности к адсорбции они расположены в так называемые лиотропные ряды. [1]
Рассмотрим вначале обмен равновалентных ионов. [2]
Обменная способность ионита при обмене равновалентных ионов не изменяется от разбавления. При обмене разновалент-ных ионов поглощение ионов с большей валентностью увеличивается по мере разбавления раствора, а сорбция ионов с меньшей валентностью уменьшается. [3]
Следовательно, обменная способность ионита при обмене равновалентных ионов не изменяется от разбавления. [4]
Рассмотрим лишь математически наиболее простой случай обмена равновалентных ионов. Примем величины л - равными величинам Ri, полагая, что обмен проводится в разбавленных растворах при условии постоянства ионной силы раствора. [5]
Из уравнения ( 9) видно, что при обмене равновалентных ионов множитель, включающий отношение объемов твердой и жидкой фаз, равен единице. [6]
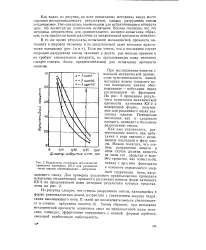 |
Результаты испытания механической. [7] |
Из рисунка следует, что степень разрушения смолы, находящейся в форме равновалентных ионов, возрастает с увеличением энергии гидратации насыщающего иона. Таким образом, при испытании механической прочности ионитовых смол по предложенной нами методике, очевидно, эффективнее оперировать с ионной формой сорбента, имеющей наибольшую набухаемость. [8]
Результаты, полученные нами ранее / 2 - 7 /, показывают, что величины а ( для обмена равновалентных ионов ( Х / С, где К - - коэффициент равновесия) для различных пар ионов щелочных металлов, как правило, заметно уменьшаются при увеличении доли более сильно сорбируемого иона. При этом изотермы ионного обмена часто имеют S - образную форму, что в соответствии с / 15 / создает известные трудности при выборе смесей ионов, которые могут быть разделены в противоточной ионообменной установке. [9]
В связи с тем, что выражение ( ZK / PK - ZR / PR) в этом случае больше, чем при обмене равновалентных ионов, In Кобм значительно больше, а адсорбция органических ионов, например, на кальциевой форме ионита всегда относительно меньше, чем на натриевой форме. [10]
Многочисленные эксперименты различных авторов показали, что кажущаяся константа обмена KAi B обычно не постоянна, а существенно меняется при изменении степени заполнения ионита даже в случае обмена равновалентных ионов. [11]
Из этой формулы следует, что чем больше ионная сила раствора, тем меньше коэффициент активности его ионов; если ионные силы двух растворов равны, то коэффициенты активности равновалентных ионов также одинаковы. В табл. 33 приведены средние значения коэффициентов активности ионов в зависимости от величины ионной силы раствора. [12]
 |
Приближенное значение средних коэффициентов активности в зависимости от ионной силы раствора. [13] |
Из этой формулы следует, что чем больше ионная сила раствора, тем меньше коэффициент активности его ионов; если ионные силы двух растворов равны, то коэффициенты активности равновалентных ионов также одинаковы. В табл. 14 приведены средние значения коэффициентов активности ионов в зависимости от величины ионной силы раствора. [14]
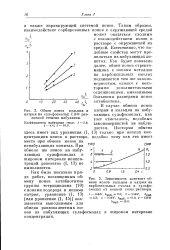 |
Обмен ионов кальция и натрия на сульфосмолах СНФ различной степени набухания.| Зависимость констант обмена ионов кальция и натрия на карбоксильных смолах и сульфосмолах от ионной силы раствора. [15] |
Страницы: 1 2