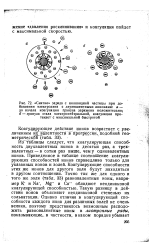
Равновалентный ион
Cтраница 2
Как было показано в ряде работ, посвященных обмену ионов антибиотиков группы тетрациклина [10] с ионами водорода и ионами натрия, уравнение ( 1, 13) [ или уравнение ( I, 15) ] оказывается выполнимым для обмена равновалентных ионов на набухающих сульфосмолах в широком интервале концентрации. [16]
Одно из основных положений, следующих из общего уравнения, состоит в том, что обменная способность ионита по отношению к одному из ионов является функцией не абсолютной концентрации ионов в растворе, а отношения активностей пары ионов, участвующих в обмене, в степенях, обратных валентностям. При обмене равновалентных ионов состав твердой фазы не изменяется с разбавлением раствора, если соотношение концентраций ( активностей) ионов в растворе остается постоянным. [17]
Применив основные допущения раздела XI. Адамсон и Гроссман [131, 132] получили уравнение кинетики обмена равновалентных ионов, учитывающее нелинейность изотермы обмена. [18]
В общем случае эта зависимость нелинейна, и сводится к линейной лишь при А О, что справедливо в случае обмена равно-валентных ионов. Таким образом, профиль концентрации коиона линеен лишь при обмене равновалентных ионов. [19]
 |
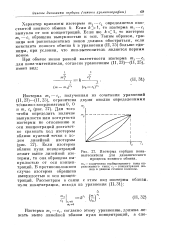
Зависимость lg - от lg - при адсорбции ионов Crs и А18. [20] |
Нами разрабатывается критерий оценки справедливости того или другого уравнения обмена для случаев равновалентных ионов. [21]
Эта установленная нами закономерность может быть объяснена, если исходить из ранее выполненных теоретических и экспериментальных исследований Гапона и Салдадзе, Самсонова [8 - 10] по изучению зависимости количества сорбированного катиона от разбавления вытеснителя и от валентности обменивающихся ионов. В соответствии с их выводами количество сорбированного иона не зависит от концентрации его в исходном растворе только при обмене равновалентных ионов. [22]
 |
Изотерма сорбции иона-вытеснителя для динамического процесса ионного обмена. [23] |
Если / с ] 1, то изотерма т1 - cl выпукла от оси концентраций. Если же k i, то изотерма т - t - сх обращена выпуклостью к оси. Таким образом, граница зон равновалентных ионов должна обостряться, если константа ионного обмена k в уравнении ( II25) больше единицы, при условии, что ион-вытеснитель является первым ионом. [24]
Из таблицы следует, что коагулирующая способность двухвалентных ионов в десятки раз, а трехвалентных - в сотни раз выше, чем у одновалентных ионов. Приведенное в таблице соотношение коагулирующих способностей ионов справедливо только для указанных ионов и золей. Точно так же для одного и того же золя ( табл. 33) равновалентные ионы, например К и Na -, Mg и Са обладают неодинаковой коагулирующей способностью. Такую разницу в действии ионов объясняют неодинаковой степенью их сольватации. [26]
Страницы: 1 2