Гарриса
Cтраница 2
Практический осмотический коэффициент рр не только не увеличивается с разбавлением, а даже иногда уменьшается, что противоречит характеру изменения свойств и ионных ассоциатов ( модель Раиса - Гарриса), и обычных низкомолекулярных сильных электролитов. Разбавление растворов полиэлектролитов сопровождается связыванием противоионов, что подтверждает большую роль электростатического поля, образованного цилиндрическим симметричным полимерным стержнем. [16]
Описано несколько приборов для ввода проб в хроматограф с помощью микропипеток. В методе Тенни и Гарриса [132] один конец пипетки вводят в хроматограф через специальное приспособление, заменяющее самоуплотняющийся дозатор, стандартный в большинстве приборов. Как только пипетку вводят в хроматограф, проба выдувается из нее газом-носителем. Такой прибор имеется в настоящее время в продаже ( фирм Fisher Scientific Со. Выпускаются пипетки объемом от 1 до 500 мкл. [17]
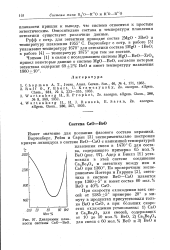 |
Диаграммы плавкости системы СаО - ВеО. [18] |
С для состава, содержащего примерно 65 мол. По проверочным экспериментам Поттера и Гарриса [2], эвтектика в системе ВеО - СаО плавится при 1360 5 и имеет состав 60 мол. [19]
Вартенберг, Ройш и Саран [5] экспериментально построили кривую ликвидуса в системе ВеО - СаО с наинизшей температурой плавления смеси 1470 для состава, содержащего примерно 65 мол. По проверочным экспериментам Поттера и Гарриса [4], эвтектика в системе ВеО - СаО плавится при 1360 5 и имеет состав 60 мол. [20]
В обеих моделях математические операции по учету отдельных факторов, влияющих на свободную энергию геля с поперечными связями, включают некоторые упрощения, ограничивающие область применения моделей. В случае модели Раиса - Гарриса уравнения содержат величины, которые нельзя измерить экспериментально. Например, степень образования ионных пар определяется с помощью удельной константы связывания, которую нельзя измерить экспериментально. Нельзя опытным путем проверить также предположение о том, что эффективная диэлектрическая константа в геле принимает минимальное значение на расстоянии 5 А от центра ионогенной группы, а при увеличении этого расстояния до 12 А линейно возрастает, пока не достигнет величины, соответствующей чистому растворителю. Для сильно набухающих гелей эта модель совсем неприменима. [21]
В обеих моделях математические операции по учету отдельных факторов, влияющих на свободную энергию геля с поперечными связями, включают некоторые упрощения, ограничивающие область применения моделей. В случае модели Раиса - Гарриса уравнения содержат величины, которые нельзя измерить экспериментально. Например, степень образования ионных пар определяется с помощью удельной константы связывания, которую нельзя измерить экспериментально. [22]
Райхенберг критически разбирает обширный и нередко противоречивый экспериментальный материал по ионообменному равновесию. Автор показывает, что теории Грегора, а также Гарриса и Раиса, сыгравшие в свое время положительную роль, не могут в настоящее время достаточно удовлетворительно объяснить явления селективности. Вслед за Рай-хенбергом следует признать прогрессивность теорий Эйзен-мана и Линга, в которых для оценки ионообменной селективности используются вполне определенные энергетические величины. [23]
 |
Термодинамические константы гидролиза иона U4. [24] |
Пятивалентное состояние урана является наименее устойчивым состоянием окисления этого элемента в растворе. Это заключение некоторое время не учитывалось, однако более поздние полярографические исследования Хила [177], Гарриса и Кольтгофа [178] полностью подтвердили существование этого иона. Дальнейшее подтверждение этой формулы по аналогии с пятивалентными ионами нептуния и америция, которым приписаны формулы NpO и AmOj, основано на кристаллографических исследованиях в инфракрасных и рентгеновых лучах. Эти исследователи обнаружили, что ион UO сравнительно устойчив в узкой области кислотности при рН, близком к 2, где диспропорционирование на U4 и UO происходит очень медленно. [25]
В последнее время появились новые экспериментальные данные, которые подтверждают найденную в опытах Штерна разность в энергиях активации реакций, приводящих к продуктам крекинга и окисления. Так, Саттерфилд и Рид [45], обрабатывая данные свои и других авторов ( Коймана, Ньюитта и Торнса, Пиза, Гарриса и Эгертона, Штерна), нашел, что эта разность в энергиях активации равна приблизительно 19 ккал / молъ. Это, несомненно, увеличивает серьезность возражения против предположения Семенова об образовании продуктов крекинга путем распада перекисных радикалов. [26]
Не решается окончательно вопрос и при предположении, что обнаруженные перекиси в подавляющей своей части состоят из перекиси водорода. Гарриса и Эгертона [9] становится понятным нахождение Ньюиттом и Торнсом большого количества перекисей ( до 20 % на сгоревший пропан) в ходе верхнетемпературного окисления. Как уже было сказано, последние авторы работали в кварцевом сосуде, причем прерывание реакции производилось погружением горячего сосуда в воду со льдом. [27]
Кусковое мыло, изготовленное из смеси мыла и синтетических веществ, широко применялось армией во время войны для стирки верхнего и нижнего белья в жесткой и даже в морской воде. В таких составах наиболее часто использовались следующие синтетические моющие средства: алкиларилсульфонаты, сульфоэтерифицированные жирные спирты и глицериды жирных кислот. По данным Гарриса, сантомерз ( нещество типа алкилбензолсульфоната) в очень жесткой и морской воде обнаруживает недостаточно сильное моющее действие. Ракман, Хьюгс и Кларк [4] разработали методы оценки моющих веществ, применяющихся в соленой воде. [28]
Недостаточность теории Грегора вытекает из модели Раиса и Гарриса [42], которые рассматривают набухание ионитов не как причину селективности, а скорее как ее побочный результат. Они объясняют набухание отталкиванием между фиксированными группами ионита и, следовательно, считают, что оно зависит от степени экранирования ( нейтрализации) фиксированных групп противоионами. По представлениям Раиса и Гарриса селективность во всех случаях обусловлена образованием ионных пар между противоионами и фиксированными группами. С ростом прочности ионных пар повышается селективность ионита по отношению к входящим в состав этих пар противоионам, но одновременно усиливается экранирование фиксированных групп и, следовательно, уменьшается набухание ионита. [29]
Вопросу селективности ионного обмена посвящены две специальные главы. Райхенберг критически разбирает обширный и нередко противоречивый экспериментальный материал по ионообменному равновесию. Автор показывает, что теории Грегора, а также Гарриса и Раиса, сыгравшие в свое время положительную роль, не могут в настоящее время достаточно удовлетворительно объяснить явления селективности. Вслед за Рай-хенбергом следует признать прогрессивность теорий Эйзен-мана и Линга, в которых для оценки ионообменной селективности используются вполне определенные энергетические величины. [30]
Страницы: 1 2 3