Подобный ион
Cтраница 3
При интерпретации порогов коагуляции для многозарядных ионов следует соблюдать некоторую осторожность, так как подобные ионы имеют тенденцию гидролизоваться и, следовательно, в действительности существуют в виде частиц с меньшей зарядностью. Например, Fe3 в значительной степени подвергается гидролизу, тогда как ион Co ( NH3) e не гидроли-зуется. [31]
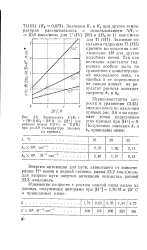 |
Зависимость k ( Ki [ Н ] ( К2 Щ ] от [ Н ] для реакции между U ( IV и Т1 ( Ш при р, 2 9 ( температура указана на кривых. [32] |
Значение энтальпии гидролиза Т1 ( III) принято по аналогии с величинами ДЯ для других подобных ионов. [33]
По данным Каминского [59], в присутствии С1 -, Вг -, Г - и других подобных ионов вязкость при повышении температуры снижается гораздо меньше, чем в их отсутствие. Очевидно, это можно связать с уменьшением размера упорядоченных кластеров молекул воды и числа водородных связей при повышении температуры. В растворах ионов, оказывающих упорядочивающее влияние на воду, условия при повышенной температуре, возможно, более благоприятны для связывания молекул воды, так как доля свободных молекул возрастает. [34]
Однозарядный ион металла М выбран ради упрощения уравнений, и этот выбор отнюдь не означает, что подобные ионы экстрагируются легче. Вследствие причин, обсуждаемых в последующей статье, некоторые комплексы трех - и двухвалентных ионов металлов экстрагируются легче. [35]
Соль Рейнеке NHiCr CNSJ NHah НзО и ее анион образуют осадки со всеми бис-циклопентадиенильными ионами, о которых мы здесь сообщали; это служит пробой на присутствие подобных ионов. [36]
Хотя при адсорбции СО2 на окиси никеля образуется ион [ СО3 ] -, этот факт сам по себе еще не является подтверждением указанной гипотезы, поскольку образования подобного иона можно было ожидать и на основании обычных химических представлений. Существенным моментом в гипотезе об образовании комплекса [ СО3 ] является то, что этот комплекс должен быть стабильным и может образоваться из любых подходящих комбинаций СО, С02 и кислорода. Попытки получить ион [ СО3 ] - с помощью методов, вытекающих из этой гипотезы, оказались неудачными. Так, например, нельзя получить ион [ СОз ] - путем обработки карбок-силатного иона кислородом. [37]
Пилотный ион, используемый в этом методе, должен быть таким, для которого свободная энергия растворения газообразного иона при 25 С одинакова во всех растворителях плюс фоновые электролиты; очевидно, найти подобный ион невозможно, но большие однозарядные катионы лучше всего подходят для этой цели. К таким ионам относятся ионы рубидия, цезия, таллия ( I), бициклопентадиенилжелеза и бициклопентадиенилко-бальта; первые три иона обратимо восстанавливаются на ртутном катоде до амальгам соответствующих металлов. Если свободная энергия растворения газообразных ионов рубидия при 25 С, как предполагают, одна и та же во всех неводных растворах, то абсолютный формальный электродный потенциал пары Rb / Rb ( Hg) будет оставаться неизменным так же, как потенциал этой пары относительно любого электрода сравнения без диффузионного потенциала. Что касается иона бициклопентадиенилжелеза, то он восстанавливается обратимо до ферроцена. Если и свободная энергия растворения газообразных нейтральных молекул, и свободная энергия растворения газообразных ионов одинакова во всех растворителях, то формальный электродный потенциал пары [ ( п - С5Н5) 2Ре ] 1 / 0 также будет оставаться неизменным. [38]
Если атом углерода в молекуле несет положительный заряд, то соединение носит название карбониевого иона если же атом углерода несет отрицательный заряд, то оно называется карб-анионом. Подобные ионы могут возникать только в качестве промежуточных соединений и присутствуют обычно лишь в очень низкой концентрации; тем не менее часто они играют решающую роль для протекания реакций, в которых они возникают. [39]
Если атом углерода в молекуле несет положительный заряд, то соединение носит название карбониевого иона; если же атом углерода несет отрицательный заряд, то оно называется карб-анионом. Подобные ионы могут возникать только в качестве промежуточных соединений и присутствуют обычно лишь в очень низкой концентрации; тем не менее часто они играют решающую роль для протекания реакций, в которых они возникают. [40]
В одном остроумном методе получения совершенной фокусировки также используется движение ионов в плоскости, перпендикулярной к магнитному полю. Все подобные ионы, которые возникают в определенной точке, должны пройти через нее после прохождения полного оборота по круговой траектории в поле независимо от массы, направления или скорости. [41]
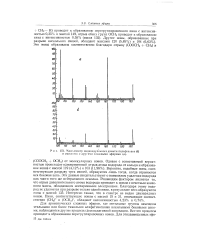 |
Масс-спектр индивидуального диметилтерефталата ( б и смеси его с другими сложными эфирами ( а. [42] |
Вероятно, подобные ионы, соответствующие разрыв) трех связей, образуются лишь тогда, когда отрывается вся боковая цепь. Эти данные свидетельствуют о возможном удалении водорода как части того же нейтрального осколка. Решающим фактором является то, что отрыв дополнительного атома водорода приводит к ионам с нечетным значением массы, обладающим неспаренными электронами. Интересно также, что в спектре не видно двузарядных ионов. [43]
Несольватировэнные ионные ассоциаты ( ионные пары) можно экстрагировать в том случае, если они состоят из ионов, имеющих достаточно большие размеры и низкие заряды. Электростатическое взаимодействие подобных ионов с водой затруднено, и все соединение легче переходит в малополярный растворитель. [44]
Во всех случаях образования комплексов комплексообразователем является катион. К числу подобных ионов относятся преимущественно катионы Со, Со, Fe, Fe, Ni, Zn, Mn, Hg, Cu, Си, Cd -, Ag, Au % Au, PtIV и др. Общим методом получения комплексов, образующихся по типу внедрения, является действие аммиака или воды на соли связываемого в комплекс иона. [45]
Страницы: 1 2 3 4