Изоэлектронный ион
Cтраница 1
Изоэлектронный ион гндроксила ОН - детально рассмотрен в гл. В этом отношении они значительно отличаются от галоидных соединений элементов пятой и шестой групп; фосфор и более тяжелые элементы образуют пентагалоидные соединения, а к шестой группе наиболее тяжелые элементы образуют тетра - и гекса-галоидные соединения, кроме соединений типа АХ3 и АХ2, соответственно. [1]
Рассмотрим изоэлектронный ион Fe ( разд. [2]
Для изоэлектронного иона V4 в кристалле А12О3 величина расщепления триплета Г ( табл. 7.11) еще меньше, чем для иона Ti3, хотя значение параметра спин-орбитального взаимодействия для свободного иона больше. Очевидно, модель статического поля лигандов является неприемлемой, и Мак-Ферлейн, Уонг и Стердж [36] ( см. также [34]) показали, что основные особенности полученных результатов могут быть объяснены с помощью динамического эффекта Яна - Теллера. Это приводит к динамическому замораживанию не только спин-орбитальной связи и орбитального момента триплета Гз, но также и расщепления, обусловленного тригональной компонентой поля лигандов. [3]
В рядах изоэлектронных ионов радиусы быстро уменьшаются при увеличении положительного заряда. [4]
 |
Поляризуемость а ( Кл - м / в и кубы радиусов г3 ( м3 некоторых ионов. [5] |
В ряду изоэлектронных ионов с конфигурацией атомов благородных газов поляризуемость растет с уменьшением положительного заряда ( например, в ряду. [6]
В спектрах изоэлектронных ионов U4, NpO и РиО2 набЛ1 Даются подобные по структуре полосы в близкой инфракрасной области. [7]
Координационное число изоэлектронного иона с меньшим радиусом иона обычно также меньше. [8]
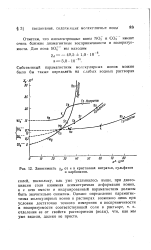 |
Зависимость у р от а в кристаллах нитратов, сульфатов. [9] |
Отметим, что изоэлектронные ионы NO3 и СОз имеют очень близкие диамагнитные восприимчивости и поляризуемости. [10]
 |
Спектр ЭПР иона. [11] |
Аналогичные расчеты для изоэлектронных ионов V2 и Мп4 указывают на увеличивающуюся разницу между вычисленными и экспериментальными значениями - факторов с ростом номинального заряда иона. Таким образом, различие между евычисл и gaKcn связано с наличием ковалент-ной связи между ионом и лигандами. [12]
Небольшие различия в энергии сольватации изоэлектронных ионов в различных растворителях являются результатом различий в энергии вторичной сольватации. Этот процесс представляет йон-дипольное взаимодействие, и его энергия зависит от заряда и размеров иона, дипольного момента молекул растворителя и его диэлектрической проницаемости. [13]
Небольшие различия в энергии сольватации изоэлектронных ионов в различных растворителях являются результатом различий в энергии вторичной сольватации. Этот процесс представляет ион-дипольное взаимодействие, и его энергия зависит от заряда и размеров иона, дипольного момента молекул растворителя и его диэлектрической проницаемости. [14]
Для ионов, содержащих одинаковое число электронов ( изоэлектронных ионов), радиус иона уменьшается с ростом его заряда. Так, в ряду S2 -, С1 -, К, Са2 радиусы равны соответственно 1 74; 1 81; 1 33; 0 99 А. [15]
Страницы: 1 2 3