Изоэлектронный ион
Cтраница 3
Необходимо упомянуть простой метод нахождения радиуса отдельного иона с той оговоркой, что вычисленные таким образом значения во многих случаях подлежат дальнейшим небольшим исправлениям для получения наиболее пригодного набора радиусов. Этот метод основан на предположении, что для пары изоэлектронных ионов, скажем Na и F, радиусы будут обратно пропорциональны эффективному ядерному заряду, воздействию которого подвергаются наружные электроны. Такое предположение следует непосредственно из выражения ( стр. [31]
 |
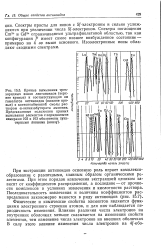
Зависимость теплоты гидратации ДЯгидр ( ккал / моль некоторых одновалентных катионов от их радиуса R ( А при t 25 С. [32] |
Для этой цели необходимо знать тепло у гидратации хотя бы одного иона. Эта задача может быть решена допущением равенства теплот гидратации изоэлектронных ионов цезия и иода. [33]
Эта зависимость использована нами для разработки нового метода нахождения энергии сольватации отдельных ионов. Метод основан на том, что разность величин энергии сольватации изоэлектронных ионов галогенов и щелочных металлов ( UCT. UCMe) с падением 1 / га2 стремится к нулю. [34]
Спектры просты для ионов с 5 / - электроном и сильно усложняются при увеличении числа 5 [ - электронов. Спектры поглощения Ст3 и Gd3 ограничиваются ультрафиолетовой областью, так как конфигурация / 7 имеет самое низшее возбужденное состояние - примерно на 4 эв выше основного. Изоэлектронные ионы обладают сходными спектрами. [36]
Учитывая большое отклонение обоих - факторов ( 4 279 и 4 1304) от - фактора свободного электрона ( 2 0023), можно считать эти два - фактора достаточно близкими и принадлежащими изоэлектронным ионам. Для изоэлектронных ионов весьма характерно, что в окружении одинаковой симметрии они дают сигналы ЭПР при сходных условиях эксперимента. Ни для Со2, ни для Fe - b при 77 К не наблюдают сигнала ЭПР; при 20 К и ниже для обоих ионов обнаруживается сильное резонансное поглощение. [37]
Значение 3 85А для расстояния Cs - J - в необнаруженной до сих пор модификации йодистого цезия со структурой хлористого натрия получено путем вычитания 2 7 % из значения, наблюдаемого для кристалла со структурой хлористого цезия; обоснование этого будет дано ниже. Размер иона при этом определяется конфигурацией внешних электронов. Для изоэлектронных ионов это распределение обратно пропорционально эффективному заряду ядра, действующему на электроны. [38]
Ожидаемое для этих молекул квадратно-пирамидальное строение подтверждено электронографическнм исследованием C1F5 [9] ( Cl - F 1 57 А), а также рентгенографически. Строение молекулы 1Р5 исследовано на примере кристаллического IF5 ( при 193 К) [ И ] ив XeF2 - IFs ( разд. Конфигурация молекулы аналогична конфигурации изоэлектронного иона XeF5 ( разд. [39]
Эффект такого сорта, как показано на фиг. Лузине, Гриффите и Вертц [83] в спектре иона Си2 в кристалле MgO; эти авторы указывали, что аналогичные явления наблюдались для иона Си2 в растворе [100]; объяснение этих явлений было предложено Мак-Коннелом [101] на основе беспорядочного движения, во многих чертах сходного с эффектом Яна - Теллера. Характерной чертой спектров как иона Си2, так и изоэлектронного иона Ni в кристалле MgO является переход к анизотропному спектру при необычно низкой температуре: изотропный спектр продолжает существовать ниже 4 К, анизотропия наступает при 1 2 К. [40]
К числу факторов, определяющих тепловой эффект, относится также заряд ядра и его поле. Сродство аммиака к протону составляет около 206 ккал. Между тем сродство отрицательного иона водорода к молекуле ВН3 с образованием изоэлектронного иона ВН4 - равно примерно 75 ккал. [41]
Из рис. 34 видна также периодичность изменения радиусов ионов. Следовательно, и для гион мы бы получили график, подобный рис. 24, а. На рис. 35, а сопоставлены значения ионных радиусов металлов основных подгрупп I и II групп периодической системы элементов, на рис. 35, б - значения гион изоэлектронных ионов щелочных металлов и галогенов. [42]
В системах такого типа из-за присутствия неподеленной пары октаэдрическая координация лигандов центрального атома должна быть искажена. Точное расположение лигандов трудно предсказать вследствие множества возможных размещений 7 электронных пар. Однако, по-видимому оно должно основываться на расположении электронных пар, соответствующем координации 1 - 3 - 3, с неподеленной парой, занимающей единственное аксиальное положение. В полимерных ионах BiBr4 -, BiI4 - и BiBr5 - 2 и мономерном ионе BiBre-3 обнаружена искаженная октаэдрическая конфигурация расположения шести лигандов вокруг атома висмута, хотя в случае полимерных ионов отклонение от ок-таэдрической симметрии может быть связано, по крайней мере частично, с наличием галогенных мостиков. Спектры комбинационного рассеяния показали, что в растворах ионы SbQ6 - 3, SbBre-3 и SbI6 - 3 имеют конфигурацию искаженного октаэдра. Однако в твердом соединении ( МН4) 2 ЬВгв, содержащем ионы SbBre-3 и SbBre -, для обоих ионов установлена конфигурация правильного октаэдра. Такое же строение в твердом состоянии имеет изоэлектронные ионы ТеХ6 - 2; эти исключения из общих правил обсуждены. [43]
Страницы: 1 2 3