Гексокиназа
Cтраница 2
Фермент, катализирующий эту реакцию, гексокиназа, а также аденозинтрифосфорная кислота имеются в дрожжах. [16]
Чтобы объяснить низкую реакционную способность воды в реакции гексокиназы теорией непродуктивного связывания, необходимо принять, что вода связывается в 2 - Ю5 раз чаще неправильно, чем правильно. Это трудно понять, поскольку для большинства химических реакций характерны много меньшие ориентационные требования. Для правильного связывания гидрок-сильного субстрата должен существовать барьер свободной энергии более чем 7 ккал / моль ( 29, ЗЛО3 Дж / моль), и энергия связывания глюкозы должна быть достаточной для преодоления этого барьера. Величина этого барьера указывает, по-видимому, на существование специфического стерического или конформационного препятствия для правильного связывания воды. [17]
В метаболизме глюкозы дрожжевых клеток участвуют два изози-ма гексокиназы. Изозимы I и II имеют одинаковую молекулярную массу - 102000 Да, состоят из двух субъединиц с молекулярной массой 52 000 Да каждая. Димеры гексокиназы могут диссоциировать на активные мономеры. При низкой концентрации белка, высокой ионной силе, а также в присутствии субстратов равновесие димерч мономер сдвигается в сторону мономера. В регуляции его активности принимает участие нуклеотидный субстрат. При постоянной концентрации ионов Mg2 и высокой концентрации АТФ наблюдается ин-гибирование фермента, при этом уменьшается максимальная скорость реакции и увеличивается константа Михаэлиса для Mg-АТФ. [18]
Магний помимо активирования определенных ферментов ( таких, как гексокиназа) играет важную роль в регулировании степени агрегации рибосомных частиц. [19]
Галактокиназа выявлена в препаратах из маша; в противоположность гексокиназе, рассмотренной на стр. УДФ-глюкозо-пирофосфорилаза получена в частично очищенном виде из проростков маша; она, по-видимому, специфична по отношению к глюкозо-1 - фосфату. Имеются данные, что значительная часть активности этого фермента связана с клеточными стенками. Галактозо-1 - фосфат-уридил-трансфераза катализирует легко обратимый перенос группы уридила между глюкозо-1 - фосфатом и галактозо-1 - фосфатом. Фермент выделен из животных тканей и из микроорганизмов; недавно получены данные о его наличии в корнях сои. УДФ-глюкозо-4-эпимераза найдена в растениях маша; подробно она изучена на препаратах, полученных из дрожжей и печени. В присутствии Т2О или Н2О18 метка в нуклео-тидах не появляется. Эти данные, а также потребность в НАД указывают на участие окислительно-восстановительного механизма. Однако выделить предполагаемый при действии этого механизма промежуточный продукт уридиндифосфо-4 - кетогексозу не удалось. [20]
При нормальной концентрации глюкозы в крови ( 5 мМ) гексокиназа полностью связана с глюкозой и работает с максимальной эффективностью, тогда как глюкокиназа насыщена лишь частично. Пока потребность мышц в глюкозо-6 - фос-фате невелика ( например, в отсутствие усиленной физической работы), повышенная концентрация глюкозо-6 - фосфата приводит к выключению гексокиназы, Таким образом, утилизация глюкозы мышцами имеет место даже в случае, когда уровень глюкозы в крови ниже нормы, но не происходит при малой потребности в глюкозо-6 - фосфате. Когда уровень глюкозы в крови нормализуется, глюкокиназа перестает работать и утилизация глюкозы печенью прекращается. [21]
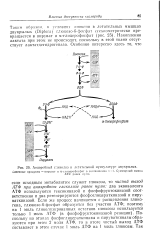 |
Анаэробный гликолиз в летательной мускулатуре двукрылых. [22] |
АТФ при анаэробном гликолизе равен нулю: два эквивалента АТФ используются гексокиназой и фосфофруктокиназой соответственно и два регенерируются фосфоглицераткиназои и пиру-ваткиназой. Поскольку на этапах фосфоглицераткиназы и пируваткиназы образуются при этом 2 моля АТФ, то в итоге чистый выход АТФ составляет в этом случае 1 моль АТФ на 1 моль глюкозы. [23]
Следовательно, можно заключить, что ограничивающие звенья в цепи гликолиза - фосфорилаза, гексокиназа, фос-фофруктокиназа функционируют одновременно как в сетчатой, так и в тканях сосудистой оболочки у новорожденных и в тех же тканях взрослого кролика. [24]
В этих условиях потребление кислорода может быть вновь активировано добавлением АДФ или глюкозы с гексокиназой. [25]
Первые результаты исследования протонной релаксации, выполненные Кон [4], свидетельствуют о том, что гексокиназа относится к типу I. Тем самым в какой-то степени поддерживается представление об упорядоченном) механи: ме. Оказалось, что усиление релаксации МпАДФ - или МпАТФ2 - наблюдается только в присутствии глюкозы. Очевидно, для выяснения механизма необходимы дальнейшие исследования. [26]
Этот энзим широко распространен и встречается в клетках всех видов; в действительности следовало бы говорить скорее о гексокиназах, чем о гексокиназе, так как, несомненно, существуют различия между гексокиназами животных клеток и более низких форм. [27]
Аналогичным образом другие ферменты могут использоваться для определения токсических веществ, Так, карбоангид-раза очень чувствительна даже к малым концентрациям хлор-производных углеводородов, гексокиназа - к хлордану, линдану и токсафену. [28]
Этот энзим широко распространен и встречается в клетках всех видов; в действительности следовало бы говорить скорее о гексокиназах, чем о гексокиназе, так как, несомненно, существуют различия между гексокиназами животных клеток и более низких форм. [29]
Различными графическими методами оценивают значения Km по глюкозе. Препарат связанной гексокиназы получают в присутствии в среде для иммобилизации 15 мМ MgCb и 5 инт. [30]
Страницы: 1 2 3 4