Карбонатный ион
Cтраница 1
Карбонатные ионы образуются в природных водах из ионов HCOJ при потере части равновесной СО2 или при усилении щелочной реакции среды. Обычно значительная часть природных вод находится в состоянии насыщения их карбонатом кальция, что имеет большое геохимическое значение и существенно для технологии обработки воды. [1]
Карбонатные ионы не могут проникать в клетки так же быстро, гак молекулы двуокиси углерода. Это положение подтверждается жспериментальными данными; ионы со своими оболочками из вод-шх молекул менее способны к проникновению через клеточную аембрану, чем нейтральные, по преимуществу липофильные, молекулы. Кроме того, в прямых опытах Остергаута и Доркаса [76] 5ыло установлено, что скорость проникновения угольной кислоты знутрь одноклеточной водоросли Valonia пропорциональна внешней концентрации двуокиси углерода, причем на нее не оказывает злияние добавление больших количеств карбонатных и бикарбо - 1атных ионов. С первого взгляда некоторые результаты Аренса 81, 85, 86 ] кажутся в противоречии с выводами Остергаута и Цоркаса. Он исследовал хорошо известный факт, что водные расте-аия, например Elodea или Potamogeton, в процессе фотосинтеза в естественных водах часто покрываются осадком карбоната кальция, в то же время вода вблизи листьев становится щелочной. Эба наблюдения легко объясняются сдвигами в равновесии (8.9), вызванном поглощением при фотосинтезе двуокиси углерода. [2]
Карбонатный ион присутствует в соляных породах в виде практически не растворимых в воде солей кальция и магния. Содержание его определяют из отдельных навесок ( см. стр. [3]
Карбонатный ион в пробах, содержащих не растворимые в воде карбонатные минералы, определяют в виде СО2 по методу Фрезениуса. [4]
Бесцветный карбонатный ион является анионом слабой, не - прочной угольной кислоты, распадающейся на ангидрид СО2 и воду в момент образования. Гидрокарбонаты щелочных, щелочноземельных и других двухвалентных металлов, а также карбонаты щелочных металлов ( и аммония) растворяются в воде. Водные растворы последних обладают сильнощелочной реакцией вследствие гидролиза. По той же причине даже КНСО3 и ЫаНСОз дают в водном растворе слабощелочную реакцию. Так как все растворимые и нерастворимые в воде карбонаты легко разлагаются кислотами ( даже слабой уксусной), то карбонатный ион обычно открывают по выделению СОз, приводящему к помутнению известковой воды. [5]
Образующийся карбонатный ион по обратной реакции связывает остаточное количество свободной углекислоты. [6]
 |
Солевой состав пластовых вод. [7] |
Гидролиз карбонатных ионов начинается выше 80 С. Для удаления накипи аппараты установки регенерации обрабатывают 2 - 10 % - й соляной кислотой с ингибитором коррозии. [8]
О типах карбонатных ионов, мигрирующих через ионообменные мембраны / Такемото; ВЦО. [9]
Увеличение концентрации карбонатных ионов ( анионов) и наличие в воде ионов кальция и магния ( катионов) способствуют, как было отмечено выше, образованию на охлаждаемой поверхности нерастворимых в воде осадков-накипи. [10]
В отсутствие карбонатного иона ( СОз -) содержание гидрокарбонатного иона ( НСОГ) в растворе совпадает с величиной общей щелочности. [11]
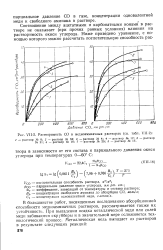 |
Растворимость СО в медноаммиачных растворах ( VII-2. [12] |
Соотношение между ацетатными и карбонатными ионами в растворе не оказывает ( при прочих равных условиях) влияния на растворимость окиси углерода. [13]
Специфическое изменение проникания карбонатных ионов представляет собой серьезную проблему, имеющую прямое отношение к повреждению мембран, обусловленному выделением карбоната кальция. [14]
Единственным окснионом углерода является карбонатный ион СОз -, а единственным стабильным окси. [15]
Страницы: 1 2 3 4