Карбонатный ион
Cтраница 2
Увеличение концентрации в воде карбонатных ионов, при наличии в воде катионов кальция, приводит к образованию осадка обладающего способностью давать плотные отложения по всему водному тракту. [16]
Поскольку и здесь исходным является карбонатный ион, то интенсивность отложения магнезиальной накипи в зависимости от биохимических и атмосферных процессов и от условий выделения СО2 из воды оказывается такой же, как и для карбонатной накипи кальция. Хильер на основании своих натурных испытаний опреснителей отмечает, что гидроокись магния образуется в небольших количествах и при температурах меньше 75 С. Однако она при этом остается в суспензии. [17]
Последний в ре-обработки обменивает свои карбонатные ионы на силикатные и трансформируется в ЗСаО А12О3 nSiO2 ( 6 - п) Н2О при п 0 15 - 0 2 - практически нерастворимый гидрогранат кальция. [18]
Таким образом, для связывания избыточных карбонатных ионов необходимо подавать известь и обрабатывать воду известью и едким натром. [19]
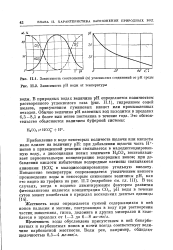 |
Зависимость соотношений ( а углекислых соединений от рН среды [ IMAGE ] Зависимость рН воды от температуры. [20] |
Щелочность воды обусловлена присутствием в ней бикарбо-натных и карбонатных ионов и почти всегда соответствует величине карбонатной жесткости. [21]
 |
Теплота адсорбции на Си20 и Ni02. [22] |
Делл и Стоун также показали, что карбонатный ион СО является стабильным в присутствии окиси углерода или кислорода. Из этого следует, что СО не может быть промежуточным продуктом в реакции окисления. Таким образом, видно, что механизмы окисления на окиси никеля и закиси меди различны. Было найдено, что С03 - комплекс устойчив при температуре 220 С, но разрушается при 350 С. Это является причиной того, что предварительная обработка окиси никеля может стать определяющим фактором в ее каталитических свойствах при кинетических исследованиях. [23]
Объясняется это тем, что при гидролизе карбонатного иона теряется молекула углекислоты. Таким образом, и вес магнезиальной накипи, образующейся в этом случае вместо карбонатной, должен составлять при прочих равных условиях лишь 58 % от веса карбонатной. Разумеется, однако, что одинаковых условий образования этих двух видов накипи быть не может. Тем не менее, если сравнить потенциальные веса карбонатной накипи 03 при температуре испарения, например, 70 С и магнезиальной накипи д 2 при температуре 80 С, то последний все же окажется меньше. [24]
Наиболее способствует ценообразованию наличие в котловой воде карбонатного иона и взвесей соединений магния. [25]
Если фенолфталеин не дает окраски, то карбонатного иона в испытуемом растворе нет и определению подлежит лишь НСОз, присутствие которого возможно ( обычно в небольших количествах) в водах и рассолах сульфатного и хлоридного типов. [26]
Щелочность известкованной воды обусловливается содержанием в растворе гидроксильных и карбонатных ионов. Повышение общей щелочности свыше 0 7 мг-экв / л указывает на передозировку известкового молока или обожженного доломита. [27]
Таким образом, силы, действующие при гидролизе карбонатных ионов в ионы гидроксила, очень малы. [28]
Если фенолфталеин не дает окраски раствора, то карбонатного иона в нем, следовательно, нет и подлежит определению лишь ион НСО3, присутствие которого возможно ( обычно в небольших количествах) в растворах второго и третьего типов. [29]
Этот способ пригоден в редких случаях, жогда количество карбонатных ионов в питательной воде равно или больше количества: иоиов кальция. [30]
Страницы: 1 2 3 4