Активность - медь
Cтраница 2
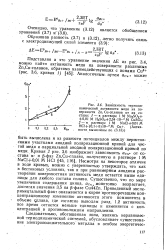
Подставляя в это уравнение значения АЕ из рис. 3.4, можно найти активность меди на поверхности различных Zn. [17]
Доказательством, могут служить отчетливо наблюдаемое повышение бестокового потенциала электрода за счет понижения активности меди при сплавообразовании V а также результаты исследования поверхности - меди методом - электронной Оже-спектроскопии. [18]
Последняя реакция, в результате которой часть уксусной кислоты восстанавливается до ацетальдегида ( ввиду слабой активности меди) протекает, однако, чрезвычайно медленно, поэтому металлическая медь является одним из важнейших материалов для изготовления оборудования, необходимого в производстве уксусной кислоты. [19]
Напротив, марганец, алюминий и некоторые другие элементы растворяются из латуни селективно, увеличивая концентрацию вакансий, активность меди и ускоряя СР цинка. [20]
Поскольку активность меди в таком расплаве должна быть незначительно меньше активности чистой меди, то очевидно, что активность меди в Cu2S немного меньше половины активности чистого элемента. [21]
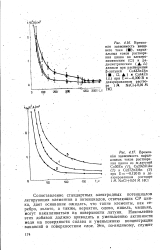
Величина удельной поверхности не является единственным фактором, обусловливающим активность меди, и это особенно четко следует из сравнения активности меди на одном и том же носителе, прокаленном при различных температурах. [22]
Результаты их работ, приведенные на рис. 15 ( активность серы) и на рис. 16 ( активности Cu2S и меди), как и следовало ожидать, показывают, что в интервале от границы растворимости к соединению Cu2S происходит крутое падение активности меди; оно происходит одновременно с резким увеличением активности серы. [23]
Чистая меДьу приготовленная из осажденйбго гидрата окиси меди и неактивная при обыкновенном давлений, оказалась кафали а-торбм ГгйДро енйзации бензбла при давлениях выше aTMbc) ip & ofo. Гидрогенизирующая активность меди чрезвьщайно зависит от присутствия примесей, особенно никеля. [24]
Сопоставление стандартных электродных потенциалов легирующих элементов и потенциалов, отвечающих СР цинка, дает основание ожидать, что такие элементы, как серебро, золото, а также, вероятно, олово, никель, мышьяк, могут накапливаться на поверхности латуни. Накопление этих добавок должно приводить к уменьшению активности меди на поверхности сплава и уменьшению концентрадии вакансий в поверхностном слое. [26]
Поэтому процесс осуществляют в подкисленном серной кислотой растворе. Кроме того, серная кислота повышает электропроводность электролита и снижает активность меди в нем, способствуя образованию мелкокристаллических осадков; однако с понижением рН заметно падает растворимость сульфата меди, что также следует иметь в виду. [27]
Например, медь, осажденная на окиси магния и на 7 - А1203, обладала более высокой активностью, чем на носителях с искаженной октаэдрической ( анатаз) или с тетраэд-рической ( силикагель, окись цинка, окись бериллия) симметрией катионных узлов. В то же время в реакции дегидрогенизации циклогексанола до цикло-гексанона активность меди, осажденной на носителях обоих типов, отличалась в меньшей степени. [28]
Однако данные по каталитической дегидрогенизации изопропилово-го спирта на исследованных металлических катализаторах не могут быть объяснены только с точки зрения незаполненности d - слоя этих катализаторов. Каталитическая активность никеля значительно выше активности платины, так же как и активность меди значительно выше активности серебра. Самый факт, что медь, не имеющая незаполненных cf - мест, является очень активным катализатором дегидрогенизации спиртов, показывает, что при помощи отдельно взятого электронного свойства - незаполненности с. [29]
Увеличение или подавление биологической активности при комплексообразовании зависит от природы донорных атомов ли-ганда, через которые осуществляется связь с медью, например координация к металлу первичных аминов резко увеличивает кроветворную активность меди. Активирующее же влияние пиридинового азота выражено несколько слабее, а при пятичленном циклообразовании с участием отрицательно заряженного кислорода активность меди подавляется. [30]
Страницы: 1 2 3 4