Активность - металл
Cтраница 2
Оценка активности металлов как поглотителей производится на основании исследования кинетики их взаимодействия с разреженными газами. Таким образом определяют скорость поглощения и величину сорбционной емкости в условиях, близких к реальной работе электровакуумного прибора. Сведения о термодинамике химических реакций, а часто и о растворении газа, получают расчетным путем из данных, относящихся к нормальным давлениям. Экспериментальной техники, пригодной для оценки теплоты и вида изостер адсорбции в вакууме, не имеется. [16]
Определение активности металла в сплаве по методу гетерогенных равновесий основано на исследовании состава равновесной смеси, состоящей из сплава, газообразной фазы и сульфида, карбида или окиси одного из компонентов сплава. [17]
Мерой активности металлов могут служить значения их стандартных электродных потенциалов ( см. стр. Электродные потенциалы малоактивных металлов ( Си, Hg, Ag, Аи и др.) выражаются положительными значениями, а более активных металлов - отрицательными. [18]
Ряды активности металлов в реакциях гидрирования этилена при 0 С и дейте-рирования при - 100 С совпадают. Значит, и в случае дейтерирования есть корреляция между активностью катализатора и процентом d - характера интерметаллической связи. [19]
 |
Определение коэффициента V - 1. [20] |
Коэффициент активности металла в сплаве ( амальгаме) определяют потенциометрически с использованием концентрационных цепей без переноса. [21]
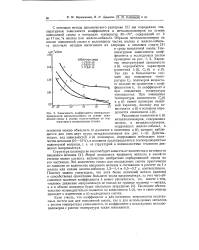 |
Зависимость коэффициента температуропроводности металлополимера на основе новолачной смолы и сплава железо-кобальт от температуры и концентрации сплава. [22] |
Мерой активности вводимого металла в какой-то степени может служить количество необратимо сорбированной смолы на его частичках. Это количество смолы для исследуемых систем практически не зависело от количества вводимого металла и составляло в расчете на 1 г железа или сплава железо-кобальта 1 3 - 1 4 и 0 5 - 0 7 г, соответственно. Последнее обстоятельство незамедлительно скажется на зависимости X ( t), что в свою очередь приведет к изменению a ( t) исследуемых систем. [23]
Как изменяется активность металлов в ряду Li - Fr и в ряду Си - Аи. [24]
Как изменяется активность металлов в ряду Fe-Со - Ni. [25]
Возможность регулировать активность металла путем соответствующего выбора процентного содержания Pt ( меньше 1 %) [103] и активность носителя введением галогена в А12О3 ( обработка НС1, HF, RC1, RF) [104] была тщательно изучена. [26]
 |
Схема возникновения электродного потенциала. [27] |
Количественная характеристика активности металлов определяется их стандартными электродными потенциалами. [28]
В ряду активности металлов олово расположено перед водородом; это неактивный металл. [29]
В ряду активности металлов свинец расположен перед водородом. Свинцовые руды находятся в СССР, в Казахстане, Восточной Сибири, Северной Осетии, на Алтае и в других местах. [30]
Страницы: 1 2 3 4