Активность - метан
Cтраница 2
Как уже было показано выше, в рассматриваемом пределе давлений концентрация метана в газовой фазе близка к единице, и, следовательно, можно считать, что коэффициент активности метана в газовой фазе равен или близок к единице. Сейдж [45] приводит пример расчета летучести метана в газовой смеси метан-м-бутан на основании экспериментальных данных по объемному поведению этой смеси. [16]
При определении коэффициентов активностей жидких углеводородов за стандартное состояние для химического потенциала было принято состояние данного углеводорода в чистом виде при тех же р и Т, что и раствор, тогда как при определении коэффициента - активности метана в жидкой фазе ( уравнение IIL8) за стандартное состояние принималось состояние бесконечного разбавления, экстраполированное на концентрацию метана, равную единице. Этим объясняется тот факт, что коэффициент активности метана в жидкой фазе меньше единицы, а коэффициент активности жидкого углеводорода в той же фазе больше единицы. [17]
Большое количество выделяющегося в результате реакции диссоциации метана углерода приводит к повышению его плотности в приповерхностной зоне, а значит к резкому снижению продолжительности жизни в активированном ( атомарном) состоянии, - происходит образование углерода в молекулярном состоянии ( сажа, кокс), науглероживающая активность метана снижается. Это приводит к необходимости ограничения содержания метана в составе газового карбюризатора - разбавлению атмосферы водяным паром или водородом. [18]
 |
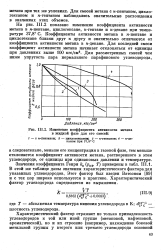
Изменение коэффициента активности метана в жидкой фазе для его смесей. [19] |
На рис. III.2 показано изменение коэффициента активности метана в w - пентане, циклогексане, к-гептане и к-декане при температуре 37 8 С. Коэффициенты активности метана в к-пентане и циклогекеане близки друг к другу и значительно отличаются от коэффициента активности метана в и-декане. [20]
При определении коэффициентов активностей жидких углеводородов за стандартное состояние для химического потенциала было принято состояние данного углеводорода в чистом виде при тех же р и Т, что и раствор, тогда как при определении коэффициента - активности метана в жидкой фазе ( уравнение IIL8) за стандартное состояние принималось состояние бесконечного разбавления, экстраполированное на концентрацию метана, равную единице. Этим объясняется тот факт, что коэффициент активности метана в жидкой фазе меньше единицы, а коэффициент активности жидкого углеводорода в той же фазе больше единицы. [21]
Для автомобилей, работающих на природном газе, целесообразно введение двух норм на выбросы углеводородов - собственно углеводородов СНХ и неметановых углеводородов NMHC. Ограничения по NMHC должны быть строгими, а по метану - более мягкими, так как парниковая активность метана по сравнению с другими углеводородами невелика. Кроме того, метан эффективно дожигается применяемыми нейтрализаторами. [22]
 |
Изменение коэффициента активности метана в жидкой фазе для его смесей. [23] |
На рис. III.2 показано изменение коэффициента активности метана в w - пентане, циклогексане, к-гептане и к-декане при температуре 37 8 С. Коэффициенты активности метана в к-пентане и циклогекеане близки друг к другу и значительно отличаются от коэффициента активности метана в и-декане. [24]
С помощью радиоактивного углерода было проверено предположение о том, что при синтезе высших углеводородов из СО и Н2 метан ( имеющийся в газовой смеси) в присутствии катализатора может входить в состав более сложных углеводородов. После нескольких часов циркуляции смеси из 50 % меченого 4С метана и 50 % СО Н2 над железным катализатором активность метана практически не изменилась, а активность окиси углерода, полученной сжиганием продуктов синтеза, была незначительной. Это значит, что метан практически не участвует в реакции. [25]
С помощью радиоактивного углерода было проверено предположение о том, что при синтезе высших углеводородов из СО и Н2 метан ( имеющийся в газовой смеси в присутствии катализатора может входить в состав более сложных углеводородов. После нескольких часов циркуляции смеси из 50 % меченого ИС метана и 50 % СО Н2 над железным катализатором активность метана практически не изменилась, а активность окиси углерода, полученной сжиганием продуктов синтеза, была незначительной. [26]
Зависимости коэффициентов активности в растворе азот-метан [1] при наиболее высокой температуре ( 122 04 К) близки к обычно наблюдаемым для зеотропных систем с неограниченной растворимостью. Отклонения от идеальности для азота меньше, чем для метана. При наиболее низкой температуре ( 99 82 К) зависимость логарифма коэффициента активности метана от концентрации перестает иметь параболический характер, а при больших концентрациях метана наблюдается характерное отклонение точек от монотонной ( по производной) зависимости. Это отклонение еще можно отнести за счет неточности экспериментальных данных или расчетной процедуры, однако активность метана, по-видимому, превышает единицу. [27]
Зависимости коэффициентов активности в растворе азот-метан [1] при наиболее высокой температуре ( 122 04 К) близки к обычно наблюдаемым для зеотропных систем с неограниченной растворимостью. Отклонения от идеальности для азота меньше, чем для метана. При наиболее низкой температуре ( 99 82 К) зависимость логарифма коэффициента активности метана от концентрации перестает иметь параболический характер, а при больших концентрациях метана наблюдается характерное отклонение точек от монотонной ( по производной) зависимости. Это отклонение еще можно отнести за счет неточности экспериментальных данных или расчетной процедуры, однако активность метана, по-видимому, превышает единицу. [28]
Страницы: 1 2