Активность - молекула
Cтраница 1
Активность молекул или ионов - это их эффективная кониент-раиия, в соответствии с которой молекулы или ионы проявляют себя в химических и физических проиессах. [1]
Активность молекул электролита й2 постоянна из-за равновесия раствора с твердым электролитом. [2]
Вообще активность молекул и агрегатов должна определяться для одинакового стандартного состояния. [3]
Однако активность молекул зависит не только от их кинетической энергии, но и от уровня энергии электронов в их атомах. Поэтому концентрация активных молекул зависит не только от температуры, но и от других факторов. К таким факторам относится прежде всего свет. [4]
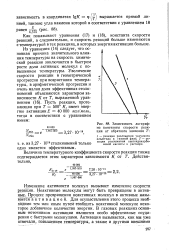 |
Зависимость логарифма константы скорости реак - 327 - Ю-18 ции от обратного значения Т. [5] |
Изменение активности молекул вызывает изменение скорости реакции. Неактивные молекулы могут быть превращены в актив-ные. Процесс превращения неактивных молекул в активные называется активацией. Для осуществления этого процесса необходимо тем или иным путем сообщить неактивной молекуле некоторое добавочное количество энергии. В газовых реакциях основный источником активации являются особо эффективные соударения с быстрыми молекулами. [6]
Понятие об активности молекул за сравнительно короткое время из чисто физического стало не просто приемлемым в химической кинетике, но необходимым. Энергия активации, начиная с 1890 - х годов, стала универсальной мерой оценки реакционной способности веществ в конкретных превращениях. [7]
При этом активность молекул воды, адсорбированных на поверхности металла, будет значительно снижена. [8]
Ацетилирование ферроцена снижает активность молекулы. [9]
Большое влияние на активность молекул могут оказывать катализаторы. [10]
Этот вид снижения люминесцентной активности молекул, как указывалось выше, может быть отнесен к случаю внутреннего тушения или тушению второго рода. [11]
Дипольный момент, характеризующий полярную активность молекул, является далеко не самым важным фактором, определяющим их смазочную эффективность. [12]
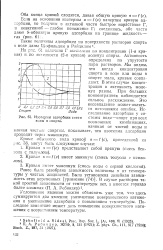 |
Изотермы адсорбции смеси воды и спирта. [13] |
В этом случае концентрация и активность молекул равны. При больших концентрациях наблюдается сильное расхождение. Это несовпадение может являться источником ошибок. [14]
По данным Шварца [157], активность молекулы пропана при атаке связи С - Н в атомах углерода, находящихся в крайнем положении, оказывается на 4 8 ккал меньше, чем при атаке связи С - Н при среднем атоме углерода. [15]
Страницы: 1 2 3 4