Активность - никель
Cтраница 3
Многие из побочных реакций, заключающихся в описанных выше реакциях восстановления, могут быть практически использованы или обойдены, если применять дезактивированный никель Ренея. Некоторые кажущиеся расхождения в описанных в химической литературе результатах обусловлены наличием или отсутствием реакций восстановления, которые сопровождают десульфуризацию; эти расхождения можно объяснить, если принять во внимание различия в условиях проведения реакции или в активности никеля Ренея; активность никеля Ренея может зависеть от времени и метода его приготовления. [31]
Многие из побочных реакций, заключающихся в описанных выше реакциях Восстановления, могут быть практически использованы или обойдены, если применять дезактивированный никель Ренея. Некоторые кажущиеся расхождения в описанных о химической литературе результатах обусловлены наличием или отсутствием реакций восстановления, которые сопровождают десульфуризацию; эти расхождения можно объяснить, если принять во внимание различия в условиях проведения реакции или в активности никеля Ренея; активность никеля PV нея можег зависеть от времени и метода его приготовления. [32]
Интересно отметить тот факт, что спектралыючистый никель, полученный из химически чистого карбоната никеля прокаливанием его в токе водорода, не активен в смысле дегидрогенизации гидроароматических соединений. Кобальт как дегидрирующий катализатор несколько менее активен, чем никель, однако он способен вызывать разложение циклогексана до метана. Активность никеля в случае дегидрирования циклогексана в бензол может быть несколько повышена прибавкой небольшого количества ( около 1 %) углекислого кальция или углекислого бария. Наибольшее повышение активности никеля достигается прибавкой окислов марганца, цинка, хром, церия, тория, алюминия или бериллия. [33]
Из предварительных результатов видно, что активность никелевого катализатора после отжига приблизительно такая же, как активность поверхности никеля после бомбардировки ионами аргона. Существенных различий в активностях отожженных и закаленных поверхностей не имеется. Активность никеля в отношении этой реакции приблизительно такая же, как и активность никеля, подтвергнутого бомбардировке ионами аргона, в отношении реакции гидрирования этилена. Активность прибора без катализатора ( фон), обусловленная наличием вольфрамовых проволок в ионизационном манометре Байяра - Альперта или никелевой пленки в той части сосуда, которая подвергается обезгаживанию, или обоими этими факторами, оказалась значительной при комнатной температуре. [34]
Ряд других элементов улучшает анодную актгп-ность никеля, среди них: Се, Cr, As, Sb, Sn, P. Однако одной из более активных добавок является cep: i. Способность серы увеличивать активность никеля хорошо известна. Никель с серой растворяется при потенциалах более отрицательных на 0 4 В, чем чистый никель. Естественно, электролиты должны содержать ионы хлора. [35]
Операцию восстановления он проводил, как правило, непосредственно в реакционной трубке, так как восстановленный никель способен легко вновь окисляться, более того, он даже пирофорен. Дальнейшие исследования Сабатье показали, что активность никеля при гидрогенизации зависит от его дисперсности и темлературы восстановления. Лишь после этого он способен гидрировать бензольное ядро. [36]
В зависимости от строения восстанавливаемого соединения он используется при температурах от 20 до 200 С и давлениях до 250 атм и более. Повышенная по сравнению с другими никелевыми катализаторами активность никеля Ренея проявляется преимущественно при гидрировании в мягких условиях. [37]
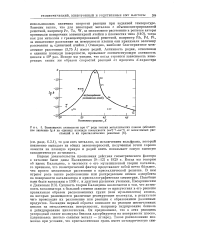 |
Зависимость активности при 0 ряда тонких металлических пленок ( абсолютное значение lg k на единицу площади поверхности ( см2 - 1-сек 1 от межатомных расстояний в их кристаллических решетках. [38] |
Очевидно, наиболее благоприятное межатомное расстояние ( 3 75 А) имеет родий. Активность родия, отнесенная к единице площади поверхности, превышает соответствующую активность никеля в 103 раз. [39]
Из предварительных результатов видно, что активность никелевого катализатора после отжига приблизительно такая же, как активность поверхности никеля после бомбардировки ионами аргона. Существенных различий в активностях отожженных и закаленных поверхностей не имеется. Активность никеля в отношении этой реакции приблизительно такая же, как и активность никеля, подтвергнутого бомбардировке ионами аргона, в отношении реакции гидрирования этилена. Активность прибора без катализатора ( фон), обусловленная наличием вольфрамовых проволок в ионизационном манометре Байяра - Альперта или никелевой пленки в той части сосуда, которая подвергается обезгаживанию, или обоими этими факторами, оказалась значительной при комнатной температуре. [40]
По своим восстановительным каталитическим свойствам кобальт подобен никелю, но по сравнению с никелем обладает меньшей активностью. Сабатье и Сандеран, изучившие гидрогенизацию в присутствии кобальта в газовой фазе, приписывают ему меньшую активность по сравнению с активностью никеля. Сравнение активности обоих металлов при восстановлении этиленовых соединений указывает на более высокую активность кобальта. Кобальт катализирует присоединение водорода по двойной связи независимо от того, находится ли она на конце цепи или же входит в цикл. [41]
Преимуществом металлов Ренея, и особенно пикеля Ренея, является то, что они, подобно катализаторам на основе благородных металлов, активны в мягких условиях. Не следует, проводить кадрирование в присутствии никеля Ренея е среде диоксапа при температурах выше 210 С, так как в этих услогищх диоксан реагирует с водородом и никелем Ренея со взрывом. При работе с никелем Ренея температура реакции снижается па 20 - 40 С по сравнению с температурой реакции в присутствии других никелевых катализаторов, Однако при 100 - 150 С активность никеля Рснея понижена. [42]
Интересно сопоставить изменение удельной каталитической активности с некоторыми другими свойствами исследованных металлов. Как видно из данных табл. 4, параметр решетки исследованных металлов четвертого периода меняется незначительно. В частности, резкое падение удельной каталитической активности при переходе от никеля ок меди нельзя объяснить увеличением параметра решетки с 2 48 до 2 55 А, так как для платины активность мало отличается от активности никеля, несмотря на увеличение параметра до 2 71 А. [43]
Интересно отметить тот факт, что спектралыючистый никель, полученный из химически чистого карбоната никеля прокаливанием его в токе водорода, не активен в смысле дегидрогенизации гидроароматических соединений. Кобальт как дегидрирующий катализатор несколько менее активен, чем никель, однако он способен вызывать разложение циклогексана до метана. Активность никеля в случае дегидрирования циклогексана в бензол может быть несколько повышена прибавкой небольшого количества ( около 1 %) углекислого кальция или углекислого бария. Наибольшее повышение активности никеля достигается прибавкой окислов марганца, цинка, хром, церия, тория, алюминия или бериллия. [44]
Очевидно, что окислы металлов ( по крайней мере в сравнительно мягких условиях) не могут служить катализаторами гидрирования окиси и двуокиси углерода. Наблюдавшееся Ипатьевым [68] превращение СО2 в метан в присутствии окиси никеля или окиси меди при давлениях выше атмосферного не является, по-видимому, достоверным. Следует думать, что в условиях эксперимента при температуре 410 - 470 С в среде, содержащей водород, окислы никеля и меди восстанавливаются, и процесс протекает на металлической поверхности. В пользу этого довода свидетельствует наблюдавшаяся автором почти одинаковая активность никеля и его окиси. [45]
Страницы: 1 2 3 4