Гелицен
Cтраница 2
Оптический выход вычислен из данных кругового дихроизма ( КД) по величине отношения g для образца и оптически чистого гелицена. [16]
При синтезе гелиценовых структур под действием циркулярно-поляризованного света [158], несмотря на малый оптический выход ( около 0 2 %), наблюдаемые вращения достигали почти 10, поскольку удельные вращения гелиценов очень велики. [17]
Двойной гелицен ( 192) был приготовлен бйе-фотоцйклизацией 2 6-бис ( 3-фенатрилэтенил) нафталина, а [13] гелицен ( 193) - из 3 6-бис ( 3-бензо [.] фенантрилэтенил) фенантрена. Был получен также [14] гелицен. [18]
Рассматривает молекулы катенанов, ротаксанов, а также полиэдранов ( см. Полиэдрические соединения), гелиценов, в к-рых неск. [19]
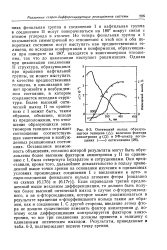 |
Оптический выход образующегося гелицена ( А, величина фактора анизотропии g ( О и УФ-спектр поглощения ( - - - - - - октагелицена. [20] |
Но теперь фенильная группа в I оказывается симметричной по отношению к этой оси и оба поворотных состояния могут выступать как предшественники ге-лицена, но исходная конформация и конформация, образующаяся при повороте на 180, находятся в энантиомерном отношении, так что до циклизации наступает рацемизация. Однако при циклизации соединения II структура, образующаяся при вращении нафтильной группы, не может выступать в качестве предшественника гелицена, и циклизация может произойти в возбужденном состоянии, в котором сохраняется исходная структура. Более высокий оптический выход II по сравнению с I может быть, таким образом, объяснен, исходя из предположения, что отношение образующихся энан-тиомеров гелицена отражает соотношение соответствующих энантиомеров в возбужденных реакционных состояниях. Оставшаяся возможность объяснения, согласно которой результаты могут быть обусловлены более высоким фактором анизотропии у II по сравнению с I, была отвергнута Бухардтом и сотрудниками. Если справедлив третий предложенный выше механизм дифференциации, то должен быть получен более высокий оптический выход в случае о-фторпроизвод-ного, а не n - фторсоединения, которое может рацемизоваться в результате вращения м-фторфенильного кольца таким же образом, как и соединение I. С другой стороны, введение атома фтора не должно существенно изменять фактор анизотропии g, поэтому если дифференциация контролируется фактором анизотропии, то все три соединения должны привести к гелицену с одинаковым оптическим выходом. Результаты, приведенные в табл. 6 - 3, подтверждают первую точку зрения. [21]
Вторая возможность состоит в том, что дифференциация имеет место как результат обратимого процесса циклизации [ первая стадия на схеме (6.15) ], сопровождаемой энантиомер-ной дифференцирующей обратимой реакцией раскрытия цикла в энантиомерном промежуточном состоянии под влиянием циркулярно-поляризованного света в качестве обратимой реакции. В этом случае остающееся промежуточное соединение становится оптически активным в стационарных условиях, и если затем происходит дегидрирование [ вторая стадия на схеме (6.15) ] с сохранением конфигурации, то в качестве продукта образуется оптически активный гелицен. [22]
Гелицен был получен в оптически активной форме при спонтанном разделении энантиомеров. Получены кинетические данные для термической рацемизации ряда гелиценов. Полагают, что термическая рацемизация представляет собою конформационный процесс, и это привело к заключению, что гелицены значительно более гибки, чем считалось. [23]
Третья возможность - это конформационная энантиомерная дифференциация исходного соединения, которое имеет спиральную хиральность, так как концевые ароматические кольца не могут находиться в одной плоскости. В этом случае один кон-формационный энантиомер диарилэтилена будет активироваться в большей степени, чем другой, и, следовательно, под влиянием циркулярно-поляризованного света в промежуточном состоянии преимущественно будет образовываться один конфигурационный энантиомер. Если конфигурация промежуточного состояния при дегидрировании сохраняется [ вторая стадия в схеме (6.15) ], то получается оптически активный гелицен. [24]
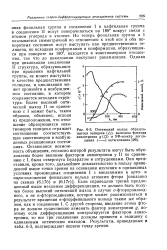 |
Оптический выход образующегося гелицена ( А, величина фактора анизотропии g ( О и УФ-спектр поглощения ( - - - - - - октагелицена. [25] |
Но теперь фенильная группа в I оказывается симметричной по отношению к этой оси и оба поворотных состояния могут выступать как предшественники ге-лицена, но исходная конформация и конформация, образующаяся при повороте на 180, находятся в энантиомерном отношении, так что до циклизации наступает рацемизация. Однако при циклизации соединения II структура, образующаяся при вращении нафтильной группы, не может выступать в качестве предшественника гелицена, и циклизация может произойти в возбужденном состоянии, в котором сохраняется исходная структура. Более высокий оптический выход II по сравнению с I может быть, таким образом, объяснен, исходя из предположения, что отношение образующихся энан-тиомеров гелицена отражает соотношение соответствующих энантиомеров в возбужденных реакционных состояниях. Оставшаяся возможность объяснения, согласно которой результаты могут быть обусловлены более высоким фактором анизотропии у II по сравнению с I, была отвергнута Бухардтом и сотрудниками. Если справедлив третий предложенный выше механизм дифференциации, то должен быть получен более высокий оптический выход в случае о-фторпроизвод-ного, а не n - фторсоединения, которое может рацемизоваться в результате вращения м-фторфенильного кольца таким же образом, как и соединение I. С другой стороны, введение атома фтора не должно существенно изменять фактор анизотропии g, поэтому если дифференциация контролируется фактором анизотропии, то все три соединения должны привести к гелицену с одинаковым оптическим выходом. Результаты, приведенные в табл. 6 - 3, подтверждают первую точку зрения. [26]
При помощи фотоциклизации можно приготовить двойные ге-лицены, которые четко разделяются на два типа. Они могут обладать одинаковой или противоположной спиральной асимметрией. В большинстве случаев гелицен является единственным циклическим продуктом. Фотоциклизация соединения ( 186) дает [8] гелицен ( 188), а из соединения ( 187) был получен [9] гелицен. [27]
При помощи фотоциклизации можно приготовить двойные ге-лицены, которые четко разделяются на два типа. Они могут обладать одинаковой или противоположной спиральной асимметрией. В большинстве случаев гелицен является единственным циклическим продуктом. Фотоциклизация соединения ( 186) дает [8] гелицен ( 188), а из соединения ( 187) был получен [9] гелицен. [28]
Структурные изомеры различаются связностью. Они отличаются с помощью топологии графа связей. Например, как показано на схеме 1 ( а), графы связей н-бутана и изобутана не являются изотопными. Однако различие в большинстве стереоизомеров вызвано некоторыми типами молекулярной жесткости. Несмотря на то что имеется очень много новых примеров стереоизомерии - от хиральных неорганических кластеров до гелиценов и битвинаненов, - они почти всегда являются просто проявлением разных типов молекулярной жесткости. Во всех таких случаях графы связей пары стереоизомеров топологически эквивалентны, даже когда уложены в трехмерном пространстве. [29]
Страницы: 1 2