Разделяемый ион
Cтраница 2
Закономерное изменение количества разделяемых ионов в равновесном растворе позволяет рассчитать состав последнего, исходя из состава раствора, применявшегося для насыщения смолы. [16]
Раствор смеси нитратов разделяемых ионов выпаривают до влажных солей. К остатку прибавляют достаточное количество смеси указанного выше состава и пропускают раствор через колонку. Вместе с висмутом на смоле сорбируются лантан и торий. [17]
Нейтральный раствор, содержащий разделяемые ионы ( лучше всего в форме хлоридов), пропускают через колонку, заполненную сильнокислотным кати-онообменннком Amberlite IR-120 в Н - форме. В этих условиях ионы Na и К не элюируются. Скорости сорбции и элюирования равны 1 см3 / мин. Для разделения смеси, содержащей 5 ммолей рассматриваемых иоиов, необходимо приблизительно 6 г смолы. Натрий можно элюировать 0 2 М НС1 в 10 % -, ном метаноле, а калий. [18]
Пусть, например, разделяемые ионы - двухзарядпые. Как известно, при обмене разнозарядных ионов увеличение концентрации раствора приводит к увеличению сорбируемости иона с меньшей величиной заряда. Поэтому, используя при фронтальном разделении в колонне / разбавленные растворы, а при вытеснении в колонне / / концентрированные, можно проводить процесс с одним и тем же вспомогательным ионом. [19]
В первом варианте все разделяемые ионы сначала поглощаются на смоле. Затем производят их разделение, пропуская через колонку со смолой раствор комплексообразователя, который раздвигает первоначально образовавшиеся близко расположенные зоны и последовательно вымывает их. Все ионы вымываются в строго определенном порядке, который задается соотношением прочности связи данного иона со смолой с прочностью образующихся в фильтрате комплексов. [20]
Электродиализом называют процесс диффузии разделяемых ионов через поры мембраны, регулируемый наложением напряжения постоянного тока. [21]
Если выходные кривые двух разделяемых ионов заметно асимметричны, то значение Р первого иона нужно рассчитывать только из нисходящей ветви, а значение Р второго ионй только и. [22]
 |
Разделение С1 -, Вг -, J - ионов. [23] |
Если количество каждого из разделяемых ионов составляет по 1 мг-экв, фракция одного галогенида содержит примесь другого порядка нескольких десятых процента. [24]
Метод разделения основан на поглощении разделяемых ионов сильнокислотным катионитом КУ-2-Na с последующей избирательной десорбцией кадмия и цинка, образующих ни-тритные анионные комплексы, раствором нитрита натрия различной концентрации. [25]
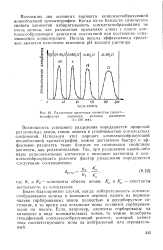 |
Разделение щелочных элементов ( ионнт. [26] |
Возможность успешного разделения определяется природой разделяемых ионов, типом ионита и устойчивостью комплексных соединений. Используя этот вариант комплексообразующей ионообменной хроматографии, можно достаточно быстро и эффективно разделять такие близкие по химическим свойствам элементы, как редкоземельные. [27]
Возможность успешного разделения определяется природой разделяемых ионов и ионита и устойчивостью комплексных соединений. Используя этот вариант комплексе-образующей ионообменной хроматографии, можно быстро и эффективно разделить такие близкие по химическим свойствам элементы, как редкоземельные и трансурановые. [28]
Сущность его заключается в различном отношении разделяемых ионов к ионитам. [29]
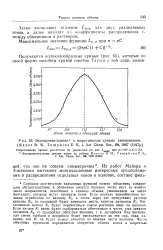 |
Экспериментальнаяа и теоретическая кривые элюирования. [ Mayer St. W., Т о m р k i n s, J. Am. Chem. Soc., 69, 2867 ( 1947. ]. [30] |
Страницы: 1 2 3 4