Акриламидный гель
Cтраница 1
Акриламидные гели обладают низкой адсорбционной способностью, поэтому при равной разрешающей способности для них характерен больший выход фракционируемого вещества, чем для гелей декстрана. [1]
 |
Разделение белков большой ММ. [2] |
ДНК они дают меньшую разрешающую способность, чем акриламидные гели. [3]
Один из типов энзимного электрода сконструирован с применением слоя акриламидного геля ( 60 - 350 мкм толщиной), в котором фиксировалась уреаза, на поверхности стеклянной мембраны. [4]
Нейхофф [5] увеличил разрешающую способность электрофо-ретического метода разделения белка, применяя более высококонцентрированный акриламидный гель с добавкой 0 5 % гидан-тоина. Нейхофф и Шилл [6] элюировали микрофракции белка, полученные этим способом, и показали, что их можно применять для иммунопреципитации. [5]
Для создания градиента рН ее помещают в стабилизированную с помощью градиента плотности или акриламидного геля среду; контакт электродов с амфолитами достигается с помощью промежуточных растворов кислот и оснований. Амфо-литы вблизи анода ( кислая среда) приобретают положительный заряд и постепенно вытесняются амфолитами с изоточкой, лежащей в более кислой области. Аналогичным образом большая часть основных амфолитов концентрируется вблизи катода, а амфолиты с промежуточными свойствами располагаются между электродами в соответствии с их изоточками. Образующийся градиент рН устойчив до тех пор, пока подается напряжение. [6]
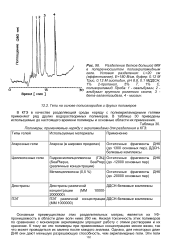
В настоящей работе приводятся первые в СССР результаты проверенных нами исследований содержания протеинов в жидких средах глаза методом разгонки в акриламидном геле. [7]
Наиболее современным, обладающим высокой разрешающей способностью и требующим малого количества материала с малым содержанием белков, является метод электрофореза в акриламидном геле. [8]
Еще лучшее разделение дает диск-электрофорез [40, 41], при котором используют дискретную ( прерывающуюся) разделительную систему из различных буферных растворов и работают с акриламидными гелями, имеющими различные размеры пор. Несколько ( минимум два) слоев геля с различными рН наслаивают один на другой, благодаря чему процессу разделения предшествует концентрирование компонентов и в результате получаются очень узкие полосы белков. [9]
 |
Изучение седиментации методом ультрацеитрифугирования ( шлирен-оптика. [10] |
Гель-зсроматографией [33 - 37] ( при работе в водной фазе - гель-фильтрацией) называется молекулярно-ситовой процесс, близкий к хроматографическим методам разделения, при котором неподвижной ( стационарной) фазой является, как правило, трехмерная структура полисахаридного или акриламидного геля. В зависимости от степени сшивки и размера пор геля, находящегося в набухшем состоянии, молекулы белка движутся через колонку с разной скоростью. При использовании геля с определенной степенью сшивки и размером пор скорость движения зависит от размера и формы молекул. Более крупные молекулы движутся в основном в пространстве между частичками геля и выходят из колонки первыми, мелкие молекулы проникают в поры геля и вследствие этого движутся значительно медленнее. [11]
 |
Амперометрические биосенсоры на основе растительных тканей. [12] |
Поскольку микроорганизмы и бактерии чувствительны к изменениям окружающей среды, для их иммобилизации используют преимущественно мягкие методы, такие как включение в гель или физическую адсорбцию. Обычно применяют акриламидные гели, желатин, коллаген, латекс натурального каучука, эфиры целлюлозы. [13]
Электроды на аспарагин и глутамин были получены также ( см. выше) иммобилизацией соответствующих ферментов на стеклянной головке катионного электрода. Электрод с иммобилизованной глутами-назой в акриламидном геле на стеклянной головке катионного электрода в соответствии с методикой, описанной Гюильбо и Монтальво [449-451], имеет нернстову зависимость потенциала от концентрации в диапазоне концентраций 10 - 4 - 10 1 М, а его время отклика равно всего 1 - 2 мин. [14]
Получение препаратов лектинов осуществляют главным образом при помощи аффинной хроматографии. Во многих случаях для этого используют сефарозу, в которую вводят моносахаридные остатки, на которых предполагают связать нужный лектин. В других случаях пользуются акриламидным гелем, который сополимеризуют с алкенил - О-гликозидами; последние должны связать лектин. Существуют и другие способы. [15]
Страницы: 1 2