Акриламидный гель
Cтраница 2
Связывание химотрипсина и глицина на сферонах семи типов приведено в табл. 8.1. Гели образуют правильные сферические гранулы и различаются по химической и физической стабильности. Они хорошо выдерживают хроматографию под давлением и не меняют свою структуру после 8-часового нагревания при 150 С в 1 М растворе гликолата натрия или после 24-часового кипячения в 20 % - ной соляной кислоте. Они биологически инертны и, подобно акриламидным гелям, не атакуются микроорганизмами. [16]
Лондон, Англия) выпускает полиакриламидные гели под названием энзакрил. Как будет показано ниже, эти акриламидные гели содержат различные функциональные группы, к которым можно присоединять различные аффинные лиганды. [17]
Большая часть иммобилизованных ферментных систем, хотя и необязательно все из них, соответствует этой схеме. Рекомендовано вводить символы ВКЛ, МИК, АДС и КСВ между названием носителя и фермента, характеризуя тем самым любой из четырех классов иммобилизованных ферментов. Так, например, трипсин, ковалентно связанный с карбоксиметилцеллюлозой, следует обозначать как КМ-целлюлоза-КСВ-тр ИПсин, уреазу, включенную в капсулу из найлона - как найлон - МИК-уреаза, а глюкоамилазу, включенную в полиакриламидный гель - как акриламидный гель - ВКЛ-глюкоамилаза. [18]
Производные полиакрилгидразид-сефарозы ведут себя как идеальные нерастворимые носители для аффинной хроматографии. Они сохраняют свойства сефарозы, в особенности минимальное неспецифическое взаимодействие с белками, хорошие фильтрующие свойства и высокую пористость. Эти производные обладают также преимуществами акриламидных гелей. [19]
Широкое распространение в некоторых странах находят различные методы включения фермента в гель. В процессе полимеризации геля молекулы фермента часто связываются, и тогда фермент оказывается заключенным внутри ячеек геля. Размеры пор геля должны быть меньше размера молекул фермента, но они не должны препятствовать доступу субстрата к ферменту. Для иммобилизации ферментов и целых клеток микроорганизмов широко используют акриламидный гель. [20]
Основным преимуществом этих разделительных матриц является их УФ-проницаемость в области длин волн ниже 260 нм. Низкая токсичность этих полимеров по сравнению с мономером акриламидом упрощает работу с этими растворами и их хранение. К тому же эти полимеры при применяемых концентрациях менее вязки, так что может проводиться их замена после каждого анализа. Однако, для некоторых длин ДНК они дают меньшую разрешающую способность, чем акриламидные гели. [22]
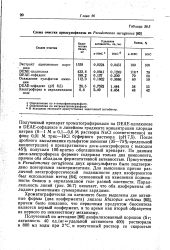 |
Схема очистки арнлсульфатазы из Pseudomonas aeruginosa [ Q3 ]. [23] |
Присутствие в Pseudomonas aeruginosa двух арилсульфатаз было подтверждено повторными экспериментами. Для выяснения причин различной электрофоретической подвижности двух изоферментов был использован метод [64], основанный на изменении подвижности белков в акриламидном геле разной плотности. [24]
Ситовой эффект проявляется наиболее ярко, когда вещества мигрируют по мембране в продольном направлении. Этот эффект особенно важен при электрофорезе в крахмальном или полиакриламидном геле. Можно вывести коэффициент, который независимо от условий электрофореза и заряда молекулы определяется исключительно ее размерами. Чем ближе цепи примыкают друг к другу, тем реже возникает возможность образования пор такого размера, через которые могли бы пройти ионы. К совершенно иным представлениям пришел Томбс [25], который подробно изучал влияние концентрации акриламидного геля на электрофоретическую подвижность. Согласно его статической модели, гель имеет четко фиксированные поры, распределение которых по размерам определяется концентрацией геля. [25]
Полученный таким путем ксерогель умеренно набухает в хлороформе и бензоле и вполне пригоден для фракционирования, например, олигомеров стирола. Полимеризацию можно также проводить в суспензии; при этом образуются сферические гранулы. Эти полимеры относительно слабо набухают в бензоле ( 90 - 150 %), но тем не менее обладают высокой пористостью. По-видимому, для этих гелей характерна гетерогенная структура ( фиг. Линейный полиакрилнитрил сшивают в мягких условиях с помощью формальдегида в 60 % - ном растворе ZnCb в присутствии серной кислоты. При этом образуются такие же мостики ( метиленбисакрил-амидные), как и при получении акриламидных гелей. [26]
Страницы: 1 2