Сульфидный ион
Cтраница 1
Сульфидный ион S2 -, гидросульфидный ион HS - и свободная H2S называются формами сероводородной кислоты. [1]
Окисление сульфидного иона из минеральных сульфидов играет важную роль в металлургии сульфидных руд. [2]
Сероводород и сульфидные ионы могут присутствовать в небольших количествах в природных водах лишь в отсутствие кислорода, окисляющего их до серы и сульфатов; существенное значение в этом процессе имеют также серобактерии. [3]
Даже при рН11 сульфидного иона остается в равновесной смеси только 0 01 % от всех форм сероводородной кислоты и уже появляется ( еще в щелочной среде. В нейтральной среде концентрация иона S2 - будет уже много меньше 0 01 %, гидросульфидного иона остается приблизительно 1 / 3 часть, а около 2 / 3 от всей сероводородной кислоты будет находиться в форме недиссоциированных молекул сероводородной кислоты, которая и может теряться благодаря улетучиванию. [4]
Следовательно, концентрация сульфидных ионов обратно пропорциональна квадрату концентрации ионов водорода в данном растворе. [5]
Влияние системы сера - сульфидный ион на величину ОкВ потенциала выявляется сильнее в отложениях древнего мидиевого ила и низов древнего мидиевого ила. Здесь ряд осадков по величине Eh располагается в пределах и вблизи теоретических значений, вычисленных из равновесия S S и ограниченных на диаграмме соответствующими линиями. Осадки же современного мидиевого ила расположены вне этих линий. [6]
Предназначен для контроля концентрации сульфидных ионов в водных растворах. [7]
Кислотный остаток сероводородной кислоты представляет собой сульфидный ион, несущий два отрицательных заряда. [8]
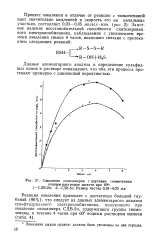 |
Омыление сополимеров с группами тиомочевины. [9] |
Данные элементарного анализа и определение сульфидных ионов в растворе показывают, что оба эти процесса протекают примерно с одинаковой вероятностью. [10]
Расчет показывает, что концентрация сульфидного иона из H2S, получающаяся в 0 3 М кислоте, достаточна для осаждения даже малых количеств элементов, входящих во И группу, но недостаточна для осаждения, элементов III группы. [11]
В сульфиде свинца PbS с сульфидным ионом связан только один ион металла. В сульфиде серебра Ag2S с одним сульфидным ионом связаны два иона металла. Следовательно, эти два металла должны иметь разные валентности. [12]
Большой интерес представляет соотношение между карбонатными и сульфидными ионами в осадках. При восстановлении сульфатов микроорганизмами в присутствии органического вещества выделяются 2 моля углекислоты и 1 моль сероводорода. [13]
Из этого уравнения видно, что сульфидный ион несет два отрицательных заряда. Определите, сколько ионов натрия должно соединиться с сульфидным ионом при образовании им натриевой соли. [14]
В 0ЗЛ / минеральной кислоте концентрация сульфидных ионов, образует - мых за счет ионизации сернистого водорода, становится настолько малой, что произведение растворимости сульфидов цинка, никеля, кобальту, же-леза и марганца не достигается, если концентрации этих элементов в растворе невелики. [15]
Страницы: 1 2 3 4