Сульфидный ион
Cтраница 2
Из этого уравнения следует, что концентрация сульфидных ионов обратно пропорциональна квадрату концентрации ионов водорода в данном растворе. [16]
Из уравнения 22 видно, что концентрация сульфидных ионов обратно пропорциональна квадрату концентрации ионов водорода. Поэтому в присутствии сильных кислот концентрация ионов S сильно уменьшается. [17]
Величины ЕЬ, вычисленные из равновесия сера - сульфидный ион, только для наиболее восстановленных осадков близки к экспериментальным. В остальных случаях разница между теоретическими и измеренными величинами большая. [18]
Из уравнения ( 22) видно, что концентрация сульфидных ионов обратно пропорциональна квадрату концентрации ионов водорода. Поэтому в присутствии сильных кислот концентрация ионов S - - сильно уменьшается. [19]
Не так заметна зависимость величины ОкВ потенциала от равновесной системы сера - сульфидный ион; разница между измеренными и вычисленными величинами Eh сравнительно большая, хотя она и меньше, чем в донном мидие-вом иле. [20]
Кроме того, как было показано Кузнецовым и Иофа [166], адсорбция сульфидных ионов увеличивает скорость анодного процесса. [21]
Сульфид меди не растворим в горячей разбавленной HCI, так как концентрация сульфидного иона в насыщенном водном растворе этого соединения столь низка, что равновесие быстро устанавливается между следами присутствующего сульфидного иона и водородным ионом, получающимся из НС1, и реакция прекращается. С другой стороны, если применяется горячая разбавленная HNO3, следы сульфидного иона постепенно удаляются благодаря окислению до свободной серы, обратная реакция не может итти, и CuS полностью растворяется. [22]
Сурьма, мышьяк, ртуть и олово ( IV) реагируют с сульфидным ионом S, образуя первоначально сульфид металла, который реагирует далее с избытком сульфидного иона, образуя растворимые комплексные ионы. [23]
Согласно нашим измерениям, осветленная вода имеет рН 12 6 и содержит, следовательно, только гидросульфидные и сульфидные ионы. При рН воды 6 1 для такого же снижения содержания сероводорода в воде требуется 5 2 м3 воздуха на 1 м3 воды. Этим объясняется тот факт, что, несмотря на интенсивную продувку карбидного ила в генераторе образующимся ацетиленом при г5 повышенной температуре, выходящий из генератора ацетилен практически не содержит сероводорода. [24]
Присоедичение новых и новых атомов серы к этому низшему полисульфидному иону может привести к образованию более высокополимерных сульфидных ионов. [25]
По Ойвину и Сусловой кожа человека и животных хорошо проницаема для недиссоциированных молекул H2S и непроницаема для сульфидных ионов, которые проникают только через поврежденную кожу. В организме H2S очень быстро окисляется до сульфатов, которые выводятся с мочой. При однократном внутривенном введении доз до 2 мг / кг через 3 - 5 мин. [26]
Из уравнения ( 4) видно, что если пренебречь изменением растворимости H2S в присутствии посторонних ионов, то концентрация сульфидных ионов обратно пропорциональна квадрату концентрации ионов водорода. Поэтому в Присутствии сильных кислот концентрация ионов S сильно уменьшается. [27]
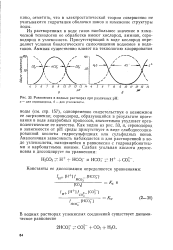 |
Равновесия в водных растворах при различных рН. а - для сероводорода, б - для углекислоты. [28] |
Как видно из рис. 33, а, сероводород в зависимости от рН среды присутствует в виде слабодиссоциированной кислоты гидросульфидных или сульфидных ионов. Аналогичная зависимость наблюдается и для растворенной в воде углекислоты, находящейся в равновесии с гидрокарбонатными и карбонатными ионами. [29]
В отличие от твердого электрода на поли - или монокристаллической основе бромидный электрод на основе жидкого ионообменника может оказаться селективным в присутствии сульфидного иона, что является весьма важным, например, при определении бромида в суль-фидсодержащих растворах. [30]
Страницы: 1 2 3 4