Реагирующий ион
Cтраница 3
Теперь S можно выразить через концентрации реагирующих ионов ( рассчитанные по содержанию изотопов в конкретном растворе), крепость кислоты, отношения соответствующих равновесных констант протонирования и отношение функций состояний для активированных комплексов, содержащих Н и D. Полученные значения R оказываются в хорошем согласии с непосредственно измеряемыми экспериментальными значениями. [31]
Для объяснения влияния заряда и размера реагирующих ионов, а также температуры и диэлектрической проницаемости среды на удельную константу скорости реакций обмена электрона между ионами были предложены различные теории. [32]
Из этого требования по ограничению концентраций реагирующих ионов металла и ли-гандов вытекают важные следствия, которые будут рассмотрены, когда мы перейдем к выбору метода определения констант устойчивости. Такие ограничения особенно значимы в случае применения малочувствительных методов, так как при работе с низкими концентрациями снижается надежность результатов. Этот вопрос будет рассмотрен в гл. [33]
Перепишите уравнение реакции, указывая только основные реагирующие ионы. [34]
Зная условную константу равновесия и исходные концентрации реагирующих ионов, можно количественно оценить полноту и - степень превращения одного осадка в другой. [35]
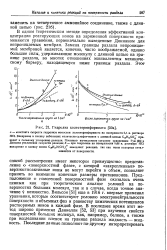 |
Гидролиз холестеринформиата [ 50а ]. [36] |
В одном теоретическом методе определения эффективной концентрации реагирующих ионов на заряженной поверхности применяются уравнения, первоначально выведенные Доннаном для непроницаемых мембран. Замена границы раздела непроницаемой мембраной является, конечно, чисто воображаемой, однако большие силы, удерживающие молекулу с длинной цепью на границе раздела, во многих отношениях эквивалентны механическому барьеру, находящемуся ниже границы раздела. [37]
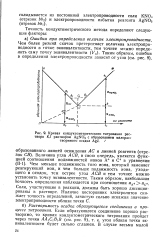 |
Кривая кондуктометрического титрования раствора KJ раствором AgNO3 с образованием малорастворимого осадка AgJ. [38] |
Чем меньше подвижность того иона, который заменяет реагирующий ион, и чем больше подвижность иона, уходящего в осадок, тем острее угол АСВ и тем точнее можно установить точку эквивалентности. Соли, участвующие в реакции, должны быть хорошо диссоциированы в растворе. Наличие посторонних электролитов снижает точность определений, зачастую сильно искажая значение электропроводности вблизи точки С. [39]
Это уравнение справедливо, если можно пренебречь миграцией реагирующих ионов и заряжением двойного электрического слоя. [40]
В общем случае электролит может содержать несколько видов реагирующих ионов, но не содержать явного избытка постороннего электролита. Расчет значений миграционных токов [ или коэффициентов а / в уравнениях типа (4.35) ] тогда очень сложен и требует использования ЭВМ. [41]
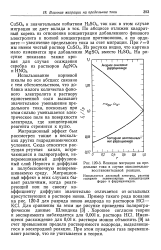 |
Влияние миграции на предельные токи в случае окислительно-восстановительной реакции. [42] |
Миграционный эффект в этих случаях бывает различным, когда реагирующий ион по своему коэффициенту диффузии значительно отличается от остальных присутствующих в растворе ионов. При этом пузырьки газа перемешивают раствор, что не учитывается в теории. [43]
Часто встречаются случаи, когда в электролите есть один реагирующий ион, концентрация которого невелика, и избыточна концентрация других ионов, не участвующих в реакции. В пределе первый член правой части уравнения (4.23) становится малым, и ион будет переноситься в основном диффузией. [44]
Величины аА, OB и аАв представляют собой активности реагирующих ионов и молекул. [45]
Страницы: 1 2 3 4