Гептафторид - иод
Cтраница 2
Способ получения фтора путем разложения комплексных соединений гептафторида иода имеет лишь препаративное значение, так как получение JF7 связано с применением фтора. [16]
Единственным представителем этого класса соединений, известным в настоящее время, является гептафторид иода, имеющий очень узкий интервал жидкого состояния. [17]
По реакционной способности галоидофториды можно расположить приблизительно в следующем порядке: трифторид хлора, пентафторид брома, гептафторид иода, монофторид хлора, трифторид брома, пентафторид иода, монофторид брома. Наиболее реакционноспособным является трифторид хлора. Большинство имеющихся в литературе данных относится только к качественной характеристике зтих веществ и в некоторых случаях не является достаточно удовлетворительным. Однако приведенные ниже данные дают некоторое представление о наиболее важных свойствах этих соединений. [18]
Окись фтора 02F2 не взаимодействует с JF5 при 90 - 195 К [82], имеет место лишь слабое разложение 02F2 на кислород и фтор; при более жестких условиях, видимо, будет происходить образование гептафторида иода. [19]
Барбенк [18] далее сообщил, что при уточнении расстояний J-F была обнаружена их неравноценность: одно из них оказалось короче ( J-F 1 71 А), чем остальные шесть, что заставляет поставить под сомнение модель пентагональной бипирамиды для молекулы гептафторида иода. [20]
Наличие при атоме углерода по меньшей мере двух атомов фтора делает инертными атомы другого галогена, в данном случае хлора. Гептафторид иода относительно медленно действует на CC12F2, но несколько энергичнее, чем фтор; авторы работы [4] полагают, что это связано с каталитическим действием иода. Однако гептафторид иода применяется для получения органических фторпроизводных лишь в редких случаях. [21]
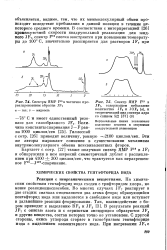 |
Спектры ЯМР F10 в частично прореагировавшем образце JF7.| Спектр ЯМР F19 в J F7, содержащем небольшие количества JF5 и JOF5 ( о, и теоретический вид спектра ядра со спином 5 / 2 ( б. [22] |
По химическим свойствам гептафторид иода сходен с трифторидом хлора, но менее реакционноспособен. Во многих случаях JF7 реагирует в две стадии: сначала отщепляются два атома фтора; образующийся пентафторид иода или выделяется в свободном виде или вступает в дальнейшие реакции фторирования. В результате реакций JF7 с окисью азота и с сернистым ангидридом образуются JF5 и другие вещества, состав которых точно не установлен. С другой стороны, окись углерода сгорает в газообразном гептафториде иода с выделением элементарного иода. [23]
Модели с симметрией С2 и Cs являются результатом статических деформаций более симметричной структуры Dik. В противоположность этому динамическая модель молекулы гептафторида иода может быть построена с помощью псевдовращения. [24]
Барбенк и Бенсей [16] на основании расчета рентгенограммы твердого гептафторида иода сделали вывод о том, что при температурах в интервале 0 - 120 СлГР7 кристал-тлизуеся в кубической фазе, которая при температуре ниже - 120 С переходит в ромбическую. Зт, отвечающая кубической модификации, достигается свободным вращением вокруг оси, расположенной с равной степенью вероятности вдоль любой из трех осей. [25]
Исходный пентафторид иода получали прямой реакцией сублимированного иода с фтором при 0 С - температуре, при которой гептафторид иода практически не образуется. Скорость реакции пента-фторида иода с фтором была рассчитана по изменению давления в реакторе со временем после смешивания реагирующих компонентов с известными парциальными давлениями. Первоначально замеряли давление парообразного JF5, затем добавляли фтор, давление которого учитывали по понижению давления в баллоне со фтором. Так как все измерения были основаны на данных давления, необходимо было показать, что концентрации связаны с давлениями законами идеальных газов. [26]
Учитывая сказанное и принимая во внимание, что в большинстве случаев F выступает как отрицательная часть молекулы, естественно галоидные соединения фтора GIF, BrF, JF называть фторидами: соответственно монофторид хлора, брома, иода. Для соединений, в которых галогены имеют валентность выше единицы, следует сохранить тот же принцип, только перед словом фторид указать количество фтора в молекуле: C1F3, BrF5, JF - соответственно трифторид хлора, пентафторид брома, гептафторид иода. [27]
Из производных фтора с другими неметаллами представляют интерес фториды галогенов. Известны гептафторид иода, все пентафториды, трифтори-ды и монофториды. Только IF не получен в чистом виде, а обнаружен в следовых количествах спектроскопически. Дело в том, что стабильность фторидов возрастает с увеличением положительной степени окисления галогенов. Поэтому наименее устойчивы монофториды. Фториды галогенов диамагнитны, так как неспаренные электроны галогенов входят в состав обобществленных электронных пар при образовании ковалентных связей с атомами фтора. [28]
Наличие при атоме углерода по меньшей мере двух атомов фтора делает инертными атомы другого галогена, в данном случае хлора. Гептафторид иода относительно медленно действует на CC12F2, но несколько энергичнее, чем фтор; авторы работы [4] полагают, что это связано с каталитическим действием иода. Однако гептафторид иода применяется для получения органических фторпроизводных лишь в редких случаях. [29]
Из производных фтора с другими неметаллами представляют интерес фториды галогенов. Известны гептафторид иода, все пентафториды, трифтори-ды и монофториды. Только IF не получен в чистом виде, а обнаружен в следовых количествах спектроскопически. Дело в том, что стабильность фторидов возрастает с увеличением положительной степени окисления галогенов. Поэтому наименее устойчивы монофториды. Фториды галогенов диамагнитны, так как неспаренные электроны галогенов входят в состав обобществленных электронных пар при образовании ковалентных связей с атомами фтора. [30]
Страницы: 1 2 3