Гептафторид - иод
Cтраница 3
Константа Трутона для JF, равна 26 4 [7]; однако расчет этой величины основан на данных теплоты сублимации, а не теплоты испарения. Это дает основание считать, что истинное значение константы Трутона должно быть ниже. Таким образом, гептафторид иода ни в газообразном, ни в жидком состоянии не проявляет свойств ассоциированного соединения. [31]
Зависимость скорости от концентрации фтора линейна, но пересечение происходит не у начала координат. Чистый гомогенный механизм обмена, а также атомный механизм авторами работы [28] отвергаются. Все атомы фтора в гептафториде иода способны к обмену. [32]
Во время перегонки сырого пентафторида иода Руфф и Кейм [21] неоднократно наблюдали выделение очень малых количеств более летучего, чем пентафторид иода, соединения, содержащего иод и фтор. Однако при нагревании смеси пентафторида иода и фтора образуется гептафторид иода. С помощью этой реакции при 250 - 270 удалось превратить в гептафторид иода 83 % исходного количества фтора. [33]
Судя по условиям реакции, автор получил пента - и гептафториды иода. [34]
Кимбел [11], исходя из теории групп, провел расчет направленной валентности применительно к различным координационным числам и для координационного числа 7 предложил структуру пентагональной бипирамиды. Даффей [12] и Скотт [13], применив метод направленных валентностей связей к молекулам и ионам типа AX7 ( JF7, ZrF7 -, NbF. Чу-Чанг Сан [14] рассчитал бипирамидальные орбиты, исходя из семиковалентных связей, и получил результаты, которые для молекулы гептафторида иода могут быть интерпретированы в пользу структуры пентагональной бипирамиды. [35]
Во время перегонки сырого пентафторида иода Руфф и Кейм [21] неоднократно наблюдали выделение очень малых количеств более летучего, чем пентафторид иода, соединения, содержащего иод и фтор. Однако при нагревании смеси пентафторида иода и фтора образуется гептафторид иода. С помощью этой реакции при 250 - 270 удалось превратить в гептафторид иода 83 % исходного количества фтора. [36]
Из производных фтора с другими неметаллами представляют интерес фториды галогенов. Последние являются интергалогенидами - межгалогенными соединениями. Атом фтора в них поляризован отрицательно, как и в случае фторидов кислорода. Известны гептафторид иода, все пентафториды, трифториды и монофториды. Только IF не получен в чистом виде, а обнаружен в следовых количествах спектроскопически. Дело в том, что стабильность фторидов возрастает с увеличением положительной степени окисления галогенов. Поэтому наименее устойчивы монофториды. Фториды галогенов диамагнитны, так как неспаренные электроны галогенов входят в состав обобществленных электронных пар при образовании ковалентных связей с атомами фтора. [37]
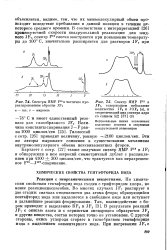 |
Спектры ЯМР F10 в частично прореагировавшем образце JF7.| Спектр ЯМР F19 в J F7, содержащем небольшие количества JF5 и JOF5 ( о, и теоретический вид спектра ядра со спином 5 / 2 ( б. [38] |
По химическим свойствам гептафторид иода сходен с трифторидом хлора, но менее реакционноспособен. Во многих случаях JF7 реагирует в две стадии: сначала отщепляются два атома фтора; образующийся пентафторид иода или выделяется в свободном виде или вступает в дальнейшие реакции фторирования. В результате реакций JF7 с окисью азота и с сернистым ангидридом образуются JF5 и другие вещества, состав которых точно не установлен. С другой стороны, окись углерода сгорает в газообразном гептафториде иода с выделением элементарного иода. [39]
Страницы: 1 2 3