Гептахлорпропан
Cтраница 1
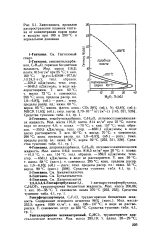 |
Зависимость пределов распространения пламени гептана от концентрации паров воды в воздухе при 100 и 200 С и нормальном давлении. [1] |
Гептахлорпропан несимметричный, С3НС17, трудногорючее кристаллическое вещество. [2]
Гептахлорпропан был получен с выходом 88 - 93 % от теории при осторожном нагревании с обратным холодильником в течение 15 час. [3]
Гептахлорпропан 153 1 2 - Дибромциклогексан 189 Дифенилдихлорметан 452 4 4 - Дифторбифенил 244 Йодистый пектаэритрит 444 енлш. [4]
По Принсу40, гептахлорпропан может быть легко выделен при выливании реакционной смеси в воду и удалении непрореагировавших исходных веществ перегонкой с паром. [5]
По Принсу40, гептахлорпропан может быть легко выделен при выливании реакционной смеси в воду и удалении непрореаги-ровавших исходных веществ перегонкой с паром. [6]
Фторирование 2Н - гептахлорпропана SbF3 / SbCl5301 302 оставляет хлорметиленовую группу незатронутой. [7]
При охлаждении остатка получают бесцветную твердую массу, которая представляет собой почти чистый гептахлорпропан. [8]
Конденсация типа Принса [103-105], примером которой может служить реакция образования симметричного гептахлорпропана в результате взаимодействия четыреххлористого углерода с трихлорэтиленом в присутствии хлористого алюминия, обычно не может быть осуществлена с фтораналогами указанных выше соединений. Однако в одном из английских патентов [74] имеется указание на возможность получения галоидалканов в результате взаимодействия галоидированного метана, содержащего по крайней мере три атома галоида ( но не фтора), с галоидированным этиленовым соединением, содержащим по крайней мере один атом фтора, в присутствии хлористого алюминия. Этим методом были приготовлены тетрахлортрифторпропан и пентахлортрифторпропан. Этот тип реакции в настоящее время для приготовления алифатических хлорфторидов почти не применяется. [9]
Так как упомянутая выше реакция необратима, то самым лучшим условием для получения гептахлорпропана является применение избытка хлороформа и возможно более низкой температуры. [10]
 |
Схема взаимного расположения боковых групп при тесной упаковке у атактического ( нерегулярного полимера стирола ( а и у изотактического полистирола ( б. [11] |
Получаемые сополимеры вулканизуют при помощи перекисей [91] или полигалогенидами, не имеющими двойных связей ( гексахлорэтап, окта-хлорциклопентан, октахлорпропан, гептахлорпропан, четыреххлористый или четырехбромистый углерод, пентабромэтан, трихлормеламин и др.), в присутствии серы. [12]
 |
Схема взаимного расположения боковых групп при тесной упаковке у атактжческого ( нерегулярного полимера стирола ( а и у изотактического полистирола ( б. [13] |
Получаемые сополимеры вулканизуют при помощи перекисей [91] или полигалогенидами, не имеющими двойных связей ( гексахлорэтан, окта-хлорциклопентан, октахлорпропан, гептахлорпропан, четыреххлористый или четырехбромистый углерод, пентабромэтан, трихлормеламин и др.), в присутствии серы. [14]
Октахлорпропан не имеет дипольного момента. Когда один атом хлора замещается водородом, то получающийся в результате гептахлорпропан имеет момент, равный 0 8D; эта величина составляет, таким образом, разницу между парциальными моментами С - С1 и С - Н связей. Однако момент хлористого пропила равен 2OD, что также можно принять за разницу между теми же самыми парциальными моментами, поскольку сам пропан вовсе лишен дипольного момента. Очевидно, в первом примере атомы хлора оказывают сильное влияние на рассматриваемую связь. Нужно ли приписать это влияние / - или D-эффекта, опять-таки трудно решить. Этот вывод совершенно естественно вытекает из основной теории / эффекта на основании следующих соображений. Это же влияние должно, однакоже, уменьшать j cci так как в паре С-С) атом хлора является богатой электронами частью. Вследствие этого величина ucci - РСЯ должна быть меньше у полихлорпропанов. [15]
Страницы: 1 2