Гиббсова
Cтраница 2
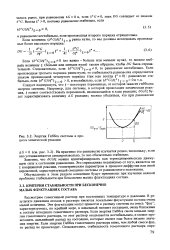 |
Энергия Гиббса системы в про-цессе химической реакции. [16] |
Следует подчеркнуть, что - некоторая переменная, от которой зависит гиббсова энергия системы. [17]
В работе [14], кроме того, было явно показано, что гиббсова термодинамика поверхностей основана на асимптотической оценке свободной энергии; а именно: члены более высокого порядка в большом потенциале Q включают отношение радиуса межмолекулярных сил к размерам системы. [18]
В большинстве случаев электронодонорные свойства заместителей по индукционному и резонансному механизмам действуют на гиббсову энергию активации в одном и том же направлении. [19]
До сих пор мы рассматривали поверхность потенциальной энергии, а в основное уравнение входит гиббсова энергия активации. В связи с этим в последние годы начали широко использовать понятие о поверхности энергии Гиббса [ ИЗ, с. Кроме того, во многих случаях можно считать, что для однотипных реакций изменения энтропии в процессе реакции приблизительно одинаковы. Это позволяет свести проблему рассмотрения поверхности энергии Гиббса к уже разобранному нами случаю, так как различия в скоростях реакций будут определяться прежде всего изменениями потенциальной энергии при переходе от одного члена рассматриваемого ряда к другому. [20]
А - площадь поперечного сечения полимерной цепи; d - длина пути перескока; ДО - гиббсова энергия активации процесса ползучести; W - доля цепей, выдерживающих прикладываемую нагрузку. [22]
Однако возможен и другой путь, использующий положение, высказанное Гиббсом [ 81 и сравнительно недавно примененное Робинсоном и Стоксом [14]: гиббсова энергия фазы не зависит от предположений, сделанных относительно числа компонентов фазы, и взаимодействий между ними. С позиций практики эта основная формула для расчета исходных коэффициентов активности должна требовать наименьшей затраты труда на вычислительные операции. С позиций теории разумно исходить из таких условий равновесия, которые обеспечили бы возможность наиболее простого вывода общей формулы для расчета коэффициентов активности. [23]
Характер упаковки молекул и силы межмолекулярных взаимодействий в различных кристаллографических плоскостях простых молекулярных кристаллов приблизительно одинаковы, поэтому одинаковой должна быть и межфазная гиббсова энергия на границе раздела расплава с различными гранями зародыша кристаллизации. [24]
Очевидно, в адсорбционных стадиях при переходе от участков с более прочными энергиями связи поверхностных соединений к участкам с менее прочными энергиями связей стандартная гиббсова энергия образования этих соединений уменьшается, а гиббсова энергия активации возрастает. [25]
Очевидно, в адсорбционных стадиях при переходе от участков с более прочными энергиями связи поверхностных соединений к участкам с менее прочными энергиями связей стандартная гиббсова энергия образования этих соединений уменьшается, а гиббсова энергия активации возрастает. [26]
Однако по мере кристаллизации изменяется конформацион-ная энтропия остатка цепи, не входящей в кристаллит, она натягивается, но это компенсируется выигрышем энергии полимерной цепи в кристалле, поэтому с ростом степени кристалличности а гиббсова энергия системы падает. [28]
Начала термодинамики ( первое и второе) в применении к таким поверхностям говорят нам о том, как связаны друг с другом при обратимом превращении изменения таких характеристических функций, как внутренняя энергия U, гиббсова свободная энергия G и объем. [29]
Поэтому, строго говоря, нельзя сосчитать гиббсову составляющую упругости тонких пленок, исходя из данных о поверхностном натяжении растворов. Подобные расчеты могут носить лишь приближенный характер. [30]
Страницы: 1 2 3

