Гибридизация - орбиталь - атом
Cтраница 2
Углы между связями отвечают sp2 - гибридизации орбиталей атомов азота и р3 - гибридизации атомов фосфора. Канонические формы составлены аналогично бензольному циклу, но в отличие от бензола л-связывание в фос-фазенах включает d - ря-взаимодействие. Это снижает устойчивость делокали-зованной молекулярной орбитали. [16]
С ростом вклада s - орбитали в гибридизацию орбиталей атома азота в продукте ( образующемся или ожидаемом), который равен 25, 33 и 50 % соответственно, повышается электроотрицательность азота, а основность амина уменьшается. Конечно, кислотность и основность определяются многими факторами, но влияние электроотрицательности весьма заметно. [17]
Современная теория для объяснения строения молекулы С6Н6 использует представление о гибридизации орбиталей атома углерода. [18]
Современная теория для объяснения строения молекулы СбН6 использует представление о гибридизации орбиталей атома углерода. [19]
Современная теория для объяснения строения молекулы СбИз использует представление о гибридизации орбиталей атома углерода. [20]
А - В, что, в свою очередь, зависит от типа гибридизации орбиталей атома А. [21]
Кампер [1], величина статического момента связи С - Н практически не зависит от гибридизации орбиталей атома С, в связи с чем, устанавливая свои данные о дипольных моментах связей, Кампер предположил, что момент связи С - - Н равен нулю. [22]
С уменьшением числа атомов в кольце углы между связями должны также уменьшаться, а при этом снижается доля s - вклада в гибридизацию орбиталей атомов цикла и в электроотрицательность кольца. [23]
Атомы кислорода в РЬО и SnO и атомы лития в LiOH имеют координационные многогранники в виде несколько искаженных тетраэдров, отвечающих 5р3 - гибридизации орбиталей атомов О. Атом свинца в структуре РЬО с четырьмя ближайшими атомами кислорода образует тетрагональную пирамиду, что можно объяснить частичным участием в связи d - орбиталей атомов РЬ. [24]
Расстояние между атомами кислорода укорочено за счет образования симметричных мостиков 0 - - - Н - - - О, причем благодаря й р2 - гибридизации орбиталей атома никеля комплекс имеет плоское строение. [25]
 |
Молекула ацетилена. [26] |
Гибридизация орбиталей затрагивает не только атом углерода. Геометрия большого числа молекул определяется гибридизацией орбиталей атомов. [27]
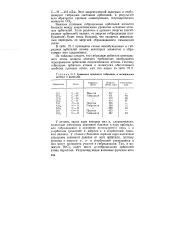 |
Сравнение прочности гибридных и негибридных молекул и радикалов. [28] |
У атомов с большим зарядом ядра валентные электроны занимают далекие от него орбитали, поэтому разница в энергии s -, p - и d - орбиталей уменьшается и они могут принимать участие в гибридизации. Так, в молекуле ВеС1а имеет место sp - гибридизация орбиталей атома бериллия. [29]
Способность фосфора расширять свой октет и переходить в пятивалентное состояние наиболее ярко выражается в таком соединении, как пятихлористый фосфор. Было показано, что это соединение имеет тригональную бипирамидальную структуру в жидкой [15] и газообразной [16] фазах, что согласуется с предложенной хр3 - гибридизацией орбиталей атома фосфора. [30]
Страницы: 1 2 3 4