Гибридизация - орбиталь - атом
Cтраница 3
Чтобы ответить на вопрос о пространственном строении молекулы, надежнее было бы воспользоваться результатами экспериментальных измерений длин связей и углов между ними. Часто, однако, пространственная структура молекул или их фрагментов может быть оценена a priori. Например, знание гибридизации орбиталей атомов, образующих молекулы и ионы, позволяет прогнозировать их форму и, наоборот, знание геометрии частиц позволяет делать выводы о гибридизации атомов, образующих эти частицы. [31]
 |
Валентные углы в молекулах водородных соединений элементов. [32] |
Энергия гибридизации ( частный случай энергии возбуждения) нередко становится определяющей в строении молекул. Энергетическим фактором, способствующим уменьшению углов, можно считать гибридизацию. Как рассчитано выше, на sp3 - гибридизацию орбиталей атома фосфора требуется 620 кДж / моль. [33]
Этот вопрос о частотах группы SC2, очевидно, заслуживает более детального изучения. Степень связи между симметричным и антисимметричным валентными колебаниями явно является функцией валентного угла группы OSO. Так как валентный угол связан также с гибридизацией орбиталей атомов серы и кислорода, то можно предполагать, что существует также некоторая зависимость между частотами и валентными углами OSO. Это действительно так, и Джиллеспай и Робинсон [33] показали, что существует приблизительно линейная зависимость между vSO ( средней) и валентным углом OSO. Они использовали полученное соотношение для определения значений валентных углов в тех соединениях, для которых эти значения были не известны. Имеется также определенная связь между разностью частот двух полос и валентным углом, но нет достаточного количества надежных данных о валентных углах, чтобы можно было проверить, дает ли этот последний метод лучшие результаты, чем соотношение Джиллеспая и Робинсона. [34]
Теория кристаллического поля предсказывает, что для частицы АВ6, где А - атом rf - элемента, находящийся в октаэдрическом поле лигандов В, при некоторых конфигурациях и спиновых состояниях атома А будет происходить малое или большое изменение длины двух аксиальных связей ( тетрагональное искажение) с образованием либо вытянутого ( чаще), либо сплющенного ( реже) вдоль выбранной оси октаэдра. В этом случае октаэдрическая частица АВ6 с йхр3г ( - гибридизацией орбиталей атома А фактически превратится в частицу АВ4 с Лр2 - гибридизацией орбиталей атома А в плоскоквадратном поле лигандов. [35]
 |
Конфигурация карбонила железа Fe ( COj5. [36] |
Здесь особый интерес представляют карбонилы типа Fe ( CO) 5, Ni ( CO) 4, где степень окисления элемента равна нулю. Пентакарбо-нил железа Fe ( СО) 5 -желтая летучая жидкость, растворимая в бензоле и эфире и нерастворимая в воде. Его молекула имеет конфигурацию тригональной бипирамиды ( рис. 83), что соответствует 5р3й - гибридизации орбиталей атома железа. [37]
 |
Типы симметрии молекул ( ионов. [38] |
Модель гибридизации электронных орбиталей не обязательно распространяют на все орбитали атома. Рассмотрим подобный случай на примере некоторых производных углерода. Известно, что строение таких соединений, как этилен С2Н4 и фосген СОС12, объясняют одинаковым характером гибридизации орбиталей атомов углерода в этих молекулах. [39]
Теория кристаллического поля предсказывает, что для частицы АВ6, где А - атом rf - элемента, находящийся в октаэдрическом поле лигандов В, при некоторых конфигурациях и спиновых состояниях атома А будет происходить малое или большое изменение длины двух аксиальных связей ( тетрагональное искажение) с образованием либо вытянутого ( чаще), либо сплющенного ( реже) вдоль выбранной оси октаэдра. В этом случае октаэдрическая частица АВ6 с йхр3г ( - гибридизацией орбиталей атома А фактически превратится в частицу АВ4 с Лр2 - гибридизацией орбиталей атома А в плоскоквадратном поле лигандов. [40]
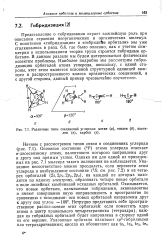 |
Различные типы соединений углерода. метан ( а, этилен ( б, ацетилен ( в, карбен ( г. [41] |
Представление о гибридизации играет важнейшую роль при описании строения неорганических и органических молекул. С понятиями гибридизация и гибридное орбитали мы уже сталкивались в разд. Наиболее подробно мы рассмотрим гибридизацию орбиталей атома углерода, поскольку, с одной стороны, этот атом является основной структурной единицей важного и распространенного класса органических соединений, а с другой стороны, данный пример чрезвычайно поучителен. [42]
 |
Различные типы соединений углерода. метан ( а, этилен ( б, ацетилен ( в, карбен ( г. [43] |
Представление о гибридизации играет важнейшую роль при описании строения неорганических и органических молекул. С понятиями гибридизация и гибридные орбитали мы уже сталкивались в разд. Наиболее подробно мы рассмотрим гибридизацию орбиталей атома углерода, поскольку, с одной стороны, этот атом является основной структурной единицей важного и распространенного класса органических соединений, а с другой стороны, данный пример чрезвычайно поучителен. [44]
Химия эфирной связи в простых эфирах в большой степени определяется поведением неподеленной пары электронов у атома кислорода. В любом случае неподеленные пары электронов образуют основной центр для присоединения протонов и кислот Льюиса и для образования оксониевых солей. Поэтому понимание химии циклических эфиров в большой степени должно зависеть от знания того, насколько нуклеофильность эфирного атома кислорода изменяется с изменением размера цикла. По-видимому, эти изменения связаны с изменениями гибридизации орбиталей атома кислорода, стерических затруднений по отношению к электрофильной атаке по атому кислорода и взаимодействий электронов орбиталей неподеленных пар с электронами орбиталей соседних атомов. [45]
Страницы: 1 2 3 4