Гидразил
Cтраница 2
В полном соответствии с критериями стабильности были получены в растворе достаточно устойчивые гидразилы XII и XVII, однако все попытки изолировать их в химически чистом виде оказались безуспешными. Роль делокализации неспэренного электрона как фактора стабилизации радикала особенно ярко - проявляется на примере гидразила XVII. Несмотря на остальные благоприятные факторы стабилизации, время полужизни радикала при 30 С составляет 30 минут. [16]
В следующей работе обнаружена линейная зависимость между константой скорости реакции замещенных гидразилов с двухвалентным железом и химическим сдвигом сигнала протона пикрильного кольца соответствующих гидразинов. [17]
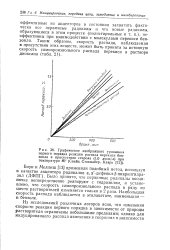 |
Графическое изображение уравнения первого порядка реакции распада перекиси бен-зоила в присутствии стирола ( 1 0 моль / л при температуре 80 ( Свейн, Стокмайер, Кларк. [18] |
Было принято, что первичные радикалы поодиночке непосредственно реагируют с гидразилом, и установлено, что скорость самопроизвольного распада в ряду из шести растворителей изменяется только в 2 раза. Наибольшая скорость распада наблюдается в этилацетате, наименьшая - в бензоле. [19]
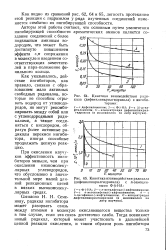 |
Кинетика взаимодействия радикала ( дифенилпикрилгидразила с ингибиторами.| Кинетика взаимодействия радикала. [20] |
Как видно из сравнений рис. 62, 64 и 65, легкость протекания этой реакции с гидразилом у ряда изученных соединений изменяется симбатно их ингибирующей способности. [21]
Уилмарт и Шварц [43] определили ряды изменения констант равновесия и констант скоростей образования геара-замещенныха а-дифенил - 3-бензоил-р - гидразилов из тетразанов в растворе ацетона при различных температурах, что позволило вычислить энергии и энтропии реакции и активации. X X Ю3 Дж / моль), а энтропия, как и следует ожидать для реакций дис-социации, сильно возрастает. Дж / моль), а энтропия активации гомолиза имеет небольшую отрицательную величину, поскольку обычно энтропия активации не учитывает изменения энтропии по координате реакции ( гл. Дж / моль) и что энтропия активации для этого процесса является сильно отрицательной, что обычно и наблюдается для реакций ассоциации ввиду значительных потерь в поступательной и вращательной энтропии. Основной причиной, обусловливающей сам факт наличия энергии активации процесса коллигации, является необходимость создания некоторой предварительной концентрации спиновой плотности на коллигирующихся атомах азота; на этот процесс оказывают влияние соседний атом азота и заместители. Влияние растворителя [40] на эти равновесные процессы будет значительно более сильным, чем влияние растворителя на равновесие гомолиза гексафенилэтана до трифенилметила ( разд. [22]
К долго живущим ( стабильным) радикалам относятся частицы, время жизни которых в растворе в инертном растворителе варьируется от нескольких минут до многих недель, месяцев или даже лет. К таким радикалам относятся триарилметилы, гидразилы, вердазилы, интроксилы, ароксилы и некоторые другие. [23]
Способы получения триарилгидразинов, основанные на взаимодействии диарилнитрозаминов с реактивами Гриньяра [6] и на реакциях металлоорганических соединений с арилазосоединениями [7], имеют менее общий характер. Кроме того, известен ряд других методов получения гидразильных радикалов, которые обычно не используют для препаративного получения гидразилов. [24]
Почти все эти радикалы устойчивы в том смысле, что они не подвержены саморазложению, однако они обратимо коллигируются, давая тетразаны. Поэтому процесс можно детально изучить. Все тетразаны, по крайней мере частично, диссоциированы в растворе на гидразилы, а некоторые из них диссоциированы полностью. После растворения тетразанов медленно устанавливалось равновесие ( часто в течение нескольких минут) при комнатной температуре, и после того, как равновесие установилось, его можно заморозить путем охлаждения до низкой температуры. Что касается реакции, то большинство радикалов более или менее медленно взаимодействует с окисью азота и трифенилметилом; но все они мгновенно восстанавливаются даже при низкой температуре гидрохиноном или гидразобензолом, образуя диарилацилгидразины. [25]
Последующие работы [90] окончательно подтвердили этот вывод. Впоследствии методом газовой хроматографии было показано [91], что ДФПГ обратимо абсорбирует кислород, а многие другие гидразилы реагируют с кислородом. [26]
Как следует из табл. 2, все ле-замещенные радикалы имеют максимум поглощения ( Хмакс) в области 500 - 508 ммк. При этом самая коротковолновая полоса отмечается у гидразила ( VII), что согласуется с ранее сделанным предположением о непланарном расположении а-нафтильного и пикрилметильного остатков в этом радикале по отношению к р-облакам а - и р-атомов азота. Что касается радикалов VII и VIII, то у них значение Ямакс меньше, чем у ДФПГ ( I), и больше, чем у II-V, что также согласуется с ранее сделанным выводом о строении этих радикалов. По всей вероятности, эта зависимость связана с ионно-радикальным равновесием исследуемых гидразилов в растворах и с тем, что окраска, очевидно, обязана наличию ионных ( а не радикальных) форм. Это подтверждается наличием парамагнетизма у растворов ДФПГ ( I), обесцвеченных трихлоруксусной кислотой. [27]
Длительные поиски единого критерия стабильности гидразилов [8, 66, 67], как и следовало ожидать, не привели к успеху, поскольку сам терм ин стабильность не имеет четкого физического смысла. Критерий равенства констант СТВ aNl aN2BO многих случаях не только не выполняется, но и не имеет никакой предсказательной силы. Наиболее полно условия, необходимые для получения стабильных радикалов, сформулированы А. Балабаном [68]: 1) стерическое экранирование атомов, несущих наибольшую спиновую плотность, 2) замена атомов водорода другими атомами в тех положениях, где может происходить диспропорционирование или димеризация и 3) максимальная делокализация неспаренного электрона. Эти чисто качественные критерии, естественно, не охватывают все многообразие факторов, определяющих устойчивость радикалов, однако, как мы увидим на примере гидразилов, выполнение этих требований способствует увеличению стабильности радикалов и позволяет целенаправленно подходить к их синтезу. [28]
Можно вырастить большие кристаллы этого радикала, изоморфные бензо-фенону, с которыми он образует смешанные кристаллы. При попытке хранить радикалы при комнатной температуре они претерпевают глубокое разложение, однако их можно длительное время хранить при температуре - М5 С. Все методы определения молекулярного веса показывают, что вещество моно-мерно даже при низких температурах. Этот радикал мгновенно восстанавливается рядом восстановителей. Он быстро соединяется с окисью азота и с три-фенилметилом, хотя продукты, первоначально образующиеся после добавления этих радикалов, претерпевают сложное разложение. Большинство из известных замещенных дифениламиноксилов обычно напоминают дифениламиноксил: они не очень устойчивые вещества. Однако некоторые радикалы этого ряда представляют исключение и гораздо более устойчивы. Эти радикалы, а также их замещенные могут храниться неопределенно долго при обычной температуре. Если на основании этих качественных выводов принять, что сопряжение с метокси - и нитро-группами оказывает стабилизующее действие, и не обращать внимания на отсутствие данных по константам равновесия, то очевидна аналогия с гидра-зилами, поскольку гидразилы, как мы видели, стабилизуются как - f - Af -, так и - АГ-заместителями. Аналогия не является полной, так как число возможных положений, в которых могут находиться заместители в аминоксилах, меньше, чем в гидразилах. [29]
Можно вырастить большие кристаллы этого радикала, изоморфные бензо-фенону, с которыми он образует смешанные кристаллы. При попытке хранить радикалы при комнатной температуре они претерпевают глубокое разложение, однако их можно длительное время хранить при температуре - М5 С. Все методы определения молекулярного веса показывают, что вещество моно-мерно даже при низких температурах. Этот радикал мгновенно восстанавливается рядом восстановителей. Он быстро соединяется с окисью азота и с три-фенилметилом, хотя продукты, первоначально образующиеся после добавления этих радикалов, претерпевают сложное разложение. Большинство из известных замещенных дифениламиноксилов обычно напоминают дифениламиноксил: они не очень устойчивые вещества. Однако некоторые радикалы этого ряда представляют исключение и гораздо более устойчивы. Эти радикалы, а также их замещенные могут храниться неопределенно долго при обычной температуре. Если на основании этих качественных выводов принять, что сопряжение с метокси - и нитро-группами оказывает стабилизующее действие, и не обращать внимания на отсутствие данных по константам равновесия, то очевидна аналогия с гидра-зилами, поскольку гидразилы, как мы видели, стабилизуются как - f - Af -, так и - АГ-заместителями. Аналогия не является полной, так как число возможных положений, в которых могут находиться заместители в аминоксилах, меньше, чем в гидразилах. [30]
Страницы: 1 2 3