Гидразон - альдегид
Cтраница 1
Гидразоны альдегидов и кетонов при нагревании со щелочью в присутствии платины выделяют азот и образуют соответствующие углеводороды. [1]
Гидразоны альдегидов также могут быть расщеплены на нитрилы амины при действии кислот или солей металлов 37, но в отличие от амино нитрильиой перегруппировки при этом требуется сильное нагревание, наблю даются побочные превращения и выходы получаются гораздо меньше. [2]
Гидразоны альдегидов и кетонов можно окислить в соответствующие диазоалканы. [3]
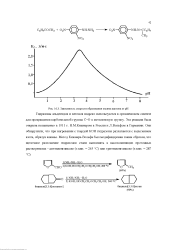 |
Зависимость скорости образования оксима ацетона от рН. [4] |
Гидразоны альдегидов и кетонов широко используются в органическом синтезе для превращения карбонильной группы СО в метиленовую группу. Они обнаружили, что при нагревании с твердой КОН гидразоны разлагаются с выделением азота, образуя алканы. [5]
Окисление гидразонов альдегидов и кетонов ( 3) И. [6]
Фишера, нагревая гидразоны альдегидов или кетонов с хлористым цинком, или по А. Е. Арбузову - нагреванием гидразонов с каталитическим количеством хлористой меди. Для получения самого индола эти реакции мало пригодны. [7]
Оказалось, что дизамещенные гидразоны альдегидов представляют собой cww - иэомеры, неспособные к превращению в йнги-формы даже при действии кислот. Производные кетонов н моно-замещенные производные альдегидов существуют в обеих ( син и анти -) формах, равновесие между которыми быстро устанавливается в растворах в присутствии следов кислот. [8]
Диметилциклобутан синтезирован разложением гидразона альдегида 1-метилциклобутан - З - карбоновой кислоты по Кижнеру. Альдегид получался каталитически в присутствии закиси марганца пропусканием паров смеси 1-метилциклобутан - З - карбоновой и муравьиной кислот ( 1: 3) через трубку с катализатором при 360 С. Выход альдегида - 60 %, считая на 1-метилциклобутан - З - карбоновую кислоту. [9]
Как показали Несмеянов, Реутов и Лосева [84-86], гидразоны альдегидов и кетонов легко реагируют с уксуснокислой ртутью при умеренной температуре ( на холоду или при 70 - 90 С) в среде воды, метанола или абсолютного бензола с выделением азота, закисных солей ртути и образованием ртутноорганических соединений, в которых ртуть находится при вторичном или третичном атоме углерода. Реакция, очевидно, проходит через промежуточное образование диазосоединений, после выделения азота, из которых происходит сопряженное присоединение ацетоксимеркургруппы по освобождающимся валентностям и, в зависимости от рода растворителя, соответствующего электроотрицательного остатка: ацетоксигруппы в случае бензола, алкоксигруппы в случае спирта, гидроксила в воде. [10]
Для стабилизации тетрахлорметана в дополнение к изложенному выше применяют смесь гидразонов альдегидов с бутилен-оксидом, тимолом и глицидолом. [11]
Альдегиды легко реагируют с гидразином уже при обы ных условиях, образуя сначала гидразон альдегида, которь: быстро конденсируется со второй молекулой альдегида в ази: Гидразоны альдегидов можно выделить только при осторол ной работе в мягких условиях с использованием избытк гидразина. [12]
Промежуточный нитрилимин ( 290) можно поймать с помощью реакции с подходящим 1 3-диполярофилом; действительно, окисление N-монозамещенных гидразонов альдегидов действием ТАС служит важным способом генерирования in situ этих интересных реакционноспособных интермедиатов. [13]
Альдегиды легко реагируют с гидразином уже при обы ных условиях, образуя сначала гидразон альдегида, которь: быстро конденсируется со второй молекулой альдегида в ази: Гидразоны альдегидов можно выделить только при осторол ной работе в мягких условиях с использованием избытк гидразина. [14]
Рассмотренные процессы относятся к реакциям циклопри-соединения ( см. разд. Будучи циклическими аналогами гидразонов альдегидов и кетонов, пиразолины, подобно последним ( см. разд. [15]
Страницы: 1 2