Гидрат - окись - магний
Cтраница 1
Гидрат окиси магния растворим в воде незначительно, но все же достаточно, чтобы сообщать фенолфталеину малиновую окраску. [2]
Гидрат окиси магния растворяется также в растворах аммонийных солей. [3]
Гидрат окиси магния очищается путем проварки в воде и в 4 - 5 % - ном растворе NaOH, карбонизуется, пропаривается и прокаливается - получается окись магния - магнезия уста. [4]
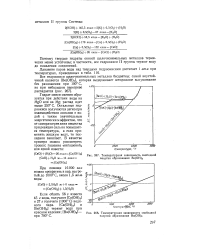 |
Температурная зависимость свободной энергии образования Ве ( ОН2.| Температурная зависимость свободно и энергии образования Ва ( ОН2. [5] |
Гидрат окиси магния образуется при действии воды на MgO или на Mg; распад идет выше 250 С. Остальные гидроокиси получаются легко при взаимодействии окислов с водой с таким значительным энергетически м эффектом, что от саморазогрев ания вещества при реакции силь но повышается температура, а если применять жидкую воду, то последняя закипает. [6]
Гидрат окиси магния отфильтровывают, тщательно промывают водой и прокаливают при невысоких температурах. В зависимости от режимов осаждения и прокаливания получаются разные сорта магнезии. Трудность получения гидроокиси магния этим способом заключается в том, что без соблюдения специальных условий осадок Mg ( OH) 2 выделяется в коллоидной форме, что сильно затрудняет его фильтрацию и промывку. Для получения легко фильтруемого осадка необходимо создать условия для медленной кристаллизации при малом пересыщении раствора и при относительно небольшом количестве центров кристаллизации. [7]
Гидрат окиси магния обладает способностью растворяться в хлористом аммоние. Последний образуется в приведенной реакции. [8]
Гидрат окиси магния растворим в воде незначительно, о все же достаточно, чтобы сообщать фенолфталеину малиновую окраску. [9]
Гидрат окиси магния растворяется также в растворах аммонийных солей. [10]
Гидрат окиси магния Mg ( OH) 2 коагулирует и выпадает в осадок. [11]
Гидрат окиси магния Mg ( OH) 2 получается при действии щелочей на MgCl2 и другие магниевые соли в виде объемистого белого студенистого осадка. Легко поглощает из воздуха углекислоту; практически нерастворим в воде. При температуре красного каления теряет воду и переходит в MgO. В природе встречается в виде минералов брусита и немалита. [12]
Гидрат окиси магния Mg ( OH) 2 встречается в природе в виде минералов б р у-сита и немалита; получается при действии щелочей на соли Mg в виде объемистого студенистого белого осадка; уд. Mg ( OH) 2 поглощает влагу и углекислоту; растворимость Mg ( OH) 2 в воде не превышает 10 мг / л, но раствор имеет явно щелочную реакцию вследствие диссоциации. [13]
Гидрат окиси магния Mg ( OH) 2 встречается в природе в виде минералов брусита и немалита. Искусственно получается при действии щелочей на растворы солей магния в виде объемистого белого студенистого осадка. Легко поглощает из воздуха двуокись углерода. Давление Н2О - над Mg ( OH) 2 при 300 равно лишь 10 лшвод. [14]
Почему гидрат окиси магния растворяется в растворе хлорида аммония. [15]
Страницы: 1 2 3 4
