Гидрат - окись - щелочной металл
Cтраница 3
Мерсер полагал, что щелочи образуют химические соединения с целлюлозой, и его взгляды разделяются и до сего времени многочисленными исследователями. Другие авторы считают, что здесь ил еет место адсорбция. Такие простейшие гидрооксисоединения, как глицерины и сахара, образуют комплексное системы с гидратами окисей щелочных металлов, щелочноземельными и тяжелыми металлами. Каррер 187 ] считает, что по аналогии целлюлоза должна вступать в соединения с едким натром. Истинный характер реакции целлюлозы с едким натром был предметом многочисленных исследований и многих споров. Поскольку по этому вопросу опубликован ряд хороших обзоров, мы остановимся на нем весьма кратко. [31]
К группе щелочных земель относятся: магний Mg кальций Са, стронций Sr и барий Ва. Щелочноземельные металлы находятся во втором вертикальном ряду периодической системы элементов. В своих соединениях они двухвалентны. Их хлориды, нитраты и сульфиды легко растворимы в воде, их гидраты окисей заметно труднее растворимы, чем гидраты окисей щелочных металлов, карбонаты же и сульфаты ( за исключением MgSO4) труднорастворимы. [32]
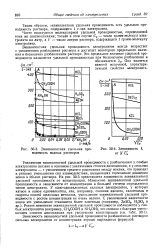 |
Эквивалентная удельная проводимость водных растворов.| Зависимость К от ] / С. [33] |
Увеличение эквивалентной удельной проводимости с разбавлением у слабых электролитов связано в основном с увеличением степени диссоциации, а у сильных электролитов - с увеличением среднего расстояния между ионами, что приводит к резкому уменьшению сил взаимодействия, вызывавших торможение движения ионов в объеме раствора. На рис. 30 - 3 представлена зависимость эквивалентной удельной проводимости от концентрации. Изменение эквивалентной удельной проводимости в зависимости от концентрации в большей степени определяется типом электролита. У одно-одновалентных сильных электролитов, у которых катион и анион одновалентны, как, например, соляная кислота, галогениды и гидраты окисей щелочных металлов, уменьшение эквивалентной удельной проводимости с ростом концентрации не очень велико. [34]
Действительно, как ужо было упомянуто, сродство молекулы аммиака к протону энергетически оценивается величиной 21.1 ккал / моль, а энергия ионной диссоциации Н2О Н ОН - - величиной 390 ккал / моль. Поэтому при образовании свободных ионов аммония и гидроксила необходима затрата энергии в 179 ккал / моль. Это количество энергии не может быть компенсировано выделением энергии электростатического притяжения свободных однозарядных ионов при связывании их в молекулу, из-за чего соединение NH4OH и не существует в твердом виде в отличие от гидратов окисей щелочных металлов, например КОН, хотя радиусы ионов К. NH весьма близки по величине. [35]
В нижеследующих таблицах собраны примеры проведения реакции Гофмана, опубликованные до сентября 1942 г. Амиды расположены по их эмпирическим формулам в порядке возрастания числа углеродных атомов. Внутри группы с одинаковым числом атомов углерода сперва помещены ( в порядке возрастания числа атомов водорода) амиды, содержащие один атом кислорода и один атом азота, затем амиды, содержащие два или больше атомов кислорода и один атом азота ( в том же порядке), затем амиды, содержащие один атом кислорода и два атома азота, и так далее. В конце помещены амиды, содержащие наряду с углеродом, водородом, кислородом и азотом также и другие элементы. Исключением являются N-бромамиды, полученные сначала в чистом виде, а потом подвергнутые перегруппировке путем обработки водной или спиртовой щелочью. Они помещены в скобках вслед за исходными амидами. Во втором столбце таблицы помещено наименование амида, в третьем указан примененный реагент. Если нет никаких других указаний, значит в качестве растворителя применялась вода и в реакционной смеси присутствовало требуемое количество гидрата окиси соответствующего щелочного металла. В случае N-бромамидов в столбце указан гидрат окиси или алкого-лят, примененный для проведения перегруппировки, причем в случае гидратов окисей растворителем служила вода, а в случае алкоголятов - соответствующий спирт. [36]
Страницы: 1 2 3